1、填空题 已知①25℃时,难溶电解质的溶度积常数:Ksp(CaC2O4)=2×10-9,②25℃时,100?mL?0.4?mol・L-1?H2C2O4水溶液中,用KOH固体来调节溶液pH(忽略体积变化),得到H2C2O4、HC2O4-、C2O42-三种微粒含量与溶液pH的变化关系如图所示。?
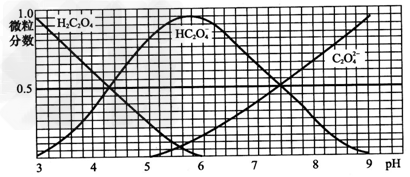
请回答下列问题:
(1)?pH=5.2时,H2C2O4、HC2O4-、C2O42-浓度从大到小依次是__________。
(2)向水中加入KHC2O4固体会使水的电离平衡向_______ 移动,解释其原因是__________。
(3)将500?mL0.2mol・L-1?H2C2O4与500?mL0.2mol・L-1 ?K2C2O4混合,关于所得溶液的下列关系式中错误的是?(? ?)
A.c(K+)>c(H+)>c(C2O42-)>c(H2C2O4)
B.c(K+)+c(H+)=2c(C2O42-)+c(HC2O4-)+c(OH-)
C.c(K+)=2c(HC2O4-)+2c(C2O42-)+2c(H2C2O4)
D.?c(C2O42-)>c(H2C2O4)>c(HC2O4-)
(4)?25℃时向1L1×10-4?moI/L?H2C2O4溶液中加入1× 10-4?mol?CaCl2固体,调节溶液pH=9,请通过计算判断是否产生白色沉淀?_________(填“是”“否”或“无法确定”)。 ?
(5)为了测定血液中的钙离子含量,通常向样品中加入K2C2O4使之转化为CaC2O4沉淀,再向过滤出的沉淀中加入 ?过量的硫酸将沉淀转化为H2C2O4,最后用高锰酸钾溶液滴定。请写出滴定时发生反应的离子方程式:_____________。
参考答案:(1)c(HC2O4-)>c(H2C2O4)>c(C2O42-)
(2)左;因为KHC2O4以电离为主,电离的H+抑制了水的电离
(3)CD
(4)是
(5)2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2+ +8H2O
本题解析:
本题难度:一般
2、选择题 下列气体通入水中,不能形成电解质溶液的是
A.NH3
B.O2
C.HBr
D.HCl
参考答案:B
本题解析:溶于水或受热熔化时能导电的化合物是电解质。氨气溶于水生成的一水合氨是电解质,溴化氢、氯化氢溶于水能电离出阴阳离子,是电解质。氧气是单质,和水不反应,溶于水后不可能形成电解质,答案是B。
本题难度:简单
3、选择题 相同温度、相同物质的量浓度的下列四种溶液
① CH3COONa ② NaHSO4 ③NaCl ④ C6H5ONa,
按pH由大到小的顺序排列正确的是
[? ]
A.④>①>③>②
B.①>③>④>②
C.①>②>③>④
D.④>③>①>②
参考答案:A
本题解析:
本题难度:一般
4、选择题 下列操作不能达到预期目的是( )
A.

检查装置气密性
B.
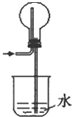
HCl的吸收
C.
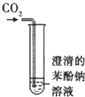
碳酸、苯酚酸性强弱比较
D.
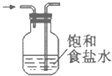
除去氯气中的氯化氢
参考答案:A.用弹簧夹夹住右边导管,向长颈漏斗中倒水,装置内外的压强不相等,液面高度不变,说明装置气密性良好,反之漏气,所以该装置能达到预期目的,故A正确;
B.该装置中,因左导管伸入烧瓶中较长,烧杯中的水进入烧瓶后不易发生倒吸,该装置既能够吸收易溶性气体,又能够防止倒吸,能吸收氯化氢,所以该装置能达到预期目的,故B正确;
C.二氧化碳通入到澄清的苯酚钠溶液中,二氧化碳和水和苯酚钠反应CO32-+2CH3COOH→2CH3COO-+H2O+CO2↑,试管中出现澄清的苯酚钠溶液变浑浊,原因是碳酸的酸性强于苯酚,水和二氧化碳反应生成碳酸,碳酸和苯酚钠反应生成苯酚和碳酸氢钠,可判断碳酸、苯酚酸性的强弱,所以该装置能达到预期目的,故C正确;
D.因氯气与水发生:Cl2+H2O?H++Cl-+HClO,则氯气难溶于饱和食盐水,但HCl极易溶于水,可用饱和食盐水除去氯气中少量的氯化氢气体,但气体进入洗气瓶时应该是长管进短管出,所以图中装置不能达到预期目的,故D错误;
故选D.
本题解析:
本题难度:简单
5、选择题 下列物质中,属于电解质的是
A.CO2
B.石墨
C.K2SO4
D.NaOH溶液
参考答案:C
本题解析:溶于水或在熔融状态下能导电的化合物是电解质,在上述条件下,均不能导电的化合物是非电解质。CO2是非电解质,A不正确;石墨是单质,不是电解质,B不正确;氢氧化钠溶液是混合物,不是电解质,D不正确,因此答案选B。
点评:判断电解质和非电解质的关键是在溶液中或在熔融状态下能不能电离出离子,能够电离出离子的化合物才是电解质,而导电只是一种现象,不能作为判断的依据。
本题难度:简单