1、计算题 I.(1)在一密闭的2L的容器里充入8mol SO2和4mol 18O2,在一定条件下开始反应:2SO2(g)+O2(g)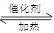 2SO3(g),2min末测得容器中有7.2mol SO2。试回答:
2SO3(g),2min末测得容器中有7.2mol SO2。试回答:
① 反应后18O原子存在于哪些物质中 ;
② 2min末SO3的浓度________________________;
③ 用O2的浓度变化表示该时间段内的化学反应速率_______________________。
II.某化学反应2A (g) B(g)+D(g)在3种不同条件下进行,B和D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在3种不同条件下进行,B和D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
实验序号
| 时间
浓度
温度
| 0
| 10
| 20
| 30
| 40
| 50
| 60
|
1
| 800℃
| 1.0
| 0.80
| 0.67
| 0.57
| 0.50
| 0.50
| 0.50
|
2
| 800℃
| c2
| 0.92
| 0.75
| 0.63
| 0.60
| 0.60
| 0.60
|
3
| 820℃
| 1.0
| 0.40
| 0.25
| 0.20
| 0.20
| 0.20
| 0.20
|
?
根据上述数据,完成下列填空:
(1) 实验1达到平衡的时间是__________min,c2_____1.0 min・L-1(填“<”“>”或“=”)。
(2)实验3比实验1的反应速率_________(填“快”或“慢”),原因是___________________________________________________________________________。
(3) 如果2A (g) B(g)+D(g)是一个吸热反应,那么实验3与实验1相比,在相同体积时___________吸收的热量多,理由是___________________________________________。
B(g)+D(g)是一个吸热反应,那么实验3与实验1相比,在相同体积时___________吸收的热量多,理由是___________________________________________。
参考答案:(12分)I.(1)①SO2、O2、SO3(2分) ?②0.4mol/L(1分)?③0.1mol/(L?min)(2分)
II.(1)40(1分)? >(1分)?
(2)快(1分)?实验3比实验1的温度高,反应速率快(2分)
(3)实验3中A的转化率大些(分解的A多些),正反应吸收热量多。(2分)
本题解析:I.(1)①首先,反应正向进行,生成的三氧化硫分子中含有18O;其次,可逆反应不仅能正向进行,也能逆向进行,三氧化硫分解产生的二氧化硫和氧气中也一定含有18O;因此,反应后中SO2、O2、SO3都含有18O;②依题意,可用三行数据法计算,即:
2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
各组分的起始浓度/ mol?L-1? 4? 2? 0
各组分的变化浓度/ mol?L-1? 0.4? 0.2? 0.4
各组分2min末浓度/ mol?L-1? 3.6? 1.8? 0.4
则2min末SO3的浓度为0.4mol/L;
③v(O2)=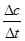 =
=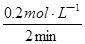 = 0.1 mol・L-1・min-1;
= 0.1 mol・L-1・min-1;
II.(1)随着反应的正向进行,反应物A的浓度逐渐减小,当A的浓度保持不变时,说明反应达到平衡,读表中信息可得,实验1中达到平衡的时间是40min;(2)实验1、2的温度相同,则平衡常数相同,先用三行数据法求实验1的平衡常数,则:
2A (g)? ?B(g)? +? D(g)
?B(g)? +? D(g)
各组分的起始浓度/ mol?L-1? 1.0? 0? 0
各组分的变化浓度/ mol?L-1? 0.50? 0.25? 0.25
各组分的平衡浓度/ mol?L-1? 0.50? 0.25? 0.25
则实验1的平衡常数K= =
=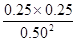 =0.25;
=0.25;
再求实验2中A的起始浓度,则:
2A (g)? ?B(g)? +? D(g)
?B(g)? +? D(g)
各组分的起始浓度/ mol?L-1? c2? 0? 0
各组分的变化浓度/ mol?L-1? c2―0.60? 0.5 c2―0.30? 0.5 c2―0.30
各组分的平衡浓度/ mol?L-1? 0.60? 0.5 c2―0.30? 0.5 c2―0.30
则实验2的平衡常数K= =
= =0.25,解得:c2="1.2" mol?L-1,则c2>1.0 mol?L-1;
=0.25,解得:c2="1.2" mol?L-1,则c2>1.0 mol?L-1;
(2)820>800,则实验3的反应速率比实验1快,因为实验3的反应温度比实验1的高;(3)实验1变为实验3,其他条件保持不变,仅升高反应温度,平衡向吸热方向移动,若2A (g)  B(g)+D(g)是一个吸热反应,则平衡向正反应方向移动,则实验3中A的转化率大于实验1中,所以实验3吸收的热量较实验1多。
B(g)+D(g)是一个吸热反应,则平衡向正反应方向移动,则实验3中A的转化率大于实验1中,所以实验3吸收的热量较实验1多。
本题难度:困难
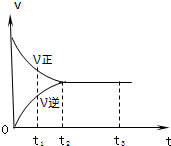
2、选择题 某条件下在密闭容器中发生反应X2+3Y2?2Z2,右图是反应过程中,反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
A.0~t1时,X2、Y2、Z2的物质的量浓度由于反应进行而减小
B.t2~t3时,反应体系中Y2的浓度没有变化
C.到t3以后,反应已达限度,不管如何改变条件,反应不再进行
D.从关系曲线可知,反应开始时体系中只有X2和Y2