沾有澄清石灰水的玻璃片
参考答案:B
本题解析:A、浓氨水与氧化钙反应有氨气放出,使蘸有浓盐酸的玻璃棒有白烟生成,正确;B、铜与浓硫酸常温下不反应,所以不会有二氧化硫生成,同时二氧化硫不与氯化钡溶液反应,常温;C、双氧水在二氧化锰作催化剂下分解生成氧气,可使代火星的木条复燃,正确;D、醋酸酸性比碳酸强,所以醋酸与碳酸氢钠溶液反应有二氧化碳气体放出,使沾有澄清石灰水的玻璃片变浑浊,正确,答案选B。
本题难度:一般
2、实验题 (每空2分,共6分)在下图所示的实验装置中,A中盛有品红溶液,B 中盛有NaOH溶液。请回答下列问题:

(1)若向A中通入足量的二氧化硫气体,A中的现象是?。
(2)如果A中盛的是浓硫酸,加入铜,加热反应,此反应中表现浓硫酸的酸性和?性。
(3)如果A中盛的是浓盐酸,加入二氧化锰,加热反应,此反应中浓盐酸的作用是?。
参考答案:37.(每空2分,共6分)(1)?红色褪去?。(2)?强氧化?。(3)?还原剂?。
本题解析:(1)SO2具有漂白性,能使品红溶液褪色。
(2)浓硫酸再加热的条件下,和铜发生氧化还原反应,生成硫酸铜、SO2和水,所以表现硫酸的氧化性和酸性。
(3)在加热的条件下,二氧化锰能氧化浓盐酸,生成氯化锰、氯气和水,所以表现盐酸的还原性和酸性。
本题难度:一般
3、选择题 浓硫酸不具有的性质是
A.吸水性
B.脱水性
C.挥发性
D.强氧化性
参考答案:C
本题解析:浓硫酸有吸水性、脱水性和强的氧化性,它的沸点较高,所以没有挥发性。选项为C。
本题难度:简单
4、选择题 银耳本身为淡黄色,有一种雪耳,颜色洁白如雪,其制作过程是:将银耳放在塑料棚内,在棚一端支个小锅,锅内放硫磺,加热使其熔化并燃烧,两天左右,雪耳就制成了,雪耳炖不烂,且对人有害,制作雪耳利用的是
A.S的还原性
B.S的漂白性
C.SO2的还原性
D.SO2的漂白性
参考答案:D
本题解析:SO2可和有色物质结合生成不稳定的物质而具有漂白性
本题难度:一般
5、实验题 测定生成SO3的转化率可以用下图装置,装置中烧瓶内发生的化学反应方程式为:Na2SO3(s)+H2SO4(85%)=Na2SO4+H2O+SO2↑(已知SO3的熔点是16.8oC,沸点是44.8oC)
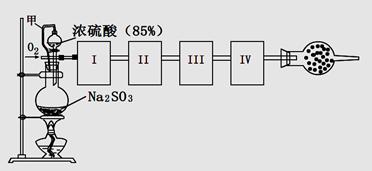
(1)装置中甲管的作用是__________________。
(2)根据实验需要,应该在I、II、III、IV处连接合适的装置,请从下图A?E装置中选择最适合装置并将其序号填至下面的空格中,每个装置不重复使用。
I、 II、III、IV处连接的装置分别是?。
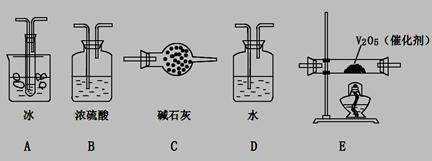
(3)为使SO2有较高的转化率,实验中加热催化剂与滴加浓硫酸的顺序中,应采取的操作是____________ ,若用大火加热烧瓶时,SO2的转化率会____________ (填“升高”、“不变”或“降低”)。
(4)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因(可以不填满)①原因:______? ②原因 :______?③原因:______
(5)将SO2通入含1mol氯酸的溶液中,可生成一种强酸和一种氧化物,并有6.02×1023个电子转移,则该反应的化学方程式为?
(6)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置IV增重了 mg,则实验中SO2的转化率为?。(用含m、n的代数式填写)
参考答案:(1)让硫酸顺利流下。(意思对,或答保持分液漏斗和烧瓶内压强相等也给分)
(2)BEAC
(3)先加热催化剂再加浓硫酸?降低
(4)①Na2SO3变质( 分),②浓硫酸的浓度不够(其他合理答案均给分)
(5)SO2+2HClO3=H2SO4+2ClO2
(6)(64n-m)/64n×100%(其他合理答案均给分)
本题解析:(1)橡胶管的作用是平衡压强,使液体顺利流下。(2)生成的二氧化硫气体通过浓硫酸干燥后通过五氧化二矾催化剂发生反应,然后将混合气体通过冰冷凝三氧化硫,二氧化硫被碱石灰吸收。(3)为提高二氧化硫转化率,催化剂应预先加热,使生成的二氧化硫立即与氧气发生反应;若大火加热,二氧化硫反应不完全,转化率低。(4)亚硫酸钠与85%硫酸反应生成二氧化硫,随着反应进行,硫酸浓度变稀,导致后续现象不明显;也可能亚硫酸钠部分变质为硫酸钠导致二氧化硫气体产生缓慢。(5)二氧化硫通过含1molHClO3溶液,转移1mol电子,说明HClO3还原产物为ClO2,所以二氧化硫被氧化为硫酸。(6)nmolNa2SO3与足量浓硫酸生成nmolSO2,装置IV增重mg说明未反应的SO2为m/64mol,所以二氧化硫转化率为(64n-m)/64n。
点评:本题实验原理是二氧化硫与氧气催化氧化生成三氧化硫,二氧化硫由亚硫酸钠与浓硫酸反应得到,最好再增加一个提供氧气的装置更好,因系统中氧气毕竟有限。
本题难度:困难
|