1、填空题 (15分)A、B、C、D、E、F六种元素分布在三个不同的短周期,他们的原子序数依次增大,其中 B与C为同一周期,A 与D,C与F分别在同一主族 ,A、D两元素原子核内的质子数之和是C、F两元素原子核内质子数之和的一半。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体,请回答下列问题:
(1)由A、B两种元素可以组成B2A4型化合物,该化合物中存在的共价键类型为是?。写出该化合物的电子式?
(2)E 是非金属元素,但能表现出一些金属元素的性质,写出E与D元素的最高价氧化物的水化物反应的离子方程式?。
(3)等浓度的ABC2溶液、HClO溶液、盐酸溶液,其导电能力:盐酸溶液>ABC2溶液>HClO溶液,则溶液的 pH (DBC2 )?pH(DClO)(填“>、<、=”)理由是?(用离子方程式解释)
(4)现有100.00mL 未知浓度的ABC2溶液,用?(仪器名称)量取10.00mL待测溶液于锥形瓶中,加入几滴?(可选指示剂:酚酞、石蕊、甲基橙),用A、C、 D三种元素组成的浓度为0.10mol/L的标准溶液来测定未知浓度的ABC2溶液,判断滴定终点的现象是?;记录消耗标准溶液的体积为12.00mL,则该ABC2溶液的浓度为mol/L;
参考答案:(1)?极性和非极性? (2分) ?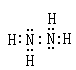 ?(2分)
?(2分)
(2)? Si + 2OH- + H2O = SiO32- + 2H2 (2分)?
(3)? < (1分)? NO2- + H2O?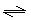 ?HNO2 +OH-?, ClO- + H2O?
?HNO2 +OH-?, ClO- + H2O?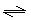 ?HClO + OH-后者水解程度大于前者(3分)
?HClO + OH-后者水解程度大于前者(3分)
(4) 酸式滴定管(1分) , 酚酞(1分) , 溶液由无色变粉红色半分钟不褪色(1分),
0.12 (2分)
本题解析:略
本题难度:一般
2、选择题 某核素的质量数为37,下列对该核素的判断可能正确的是( ?)
?
| A
| B
| C
| D
|
质子数
| 18
| 17
| 19
| 17
|
中子数
| 19
| 17
| 18
| 20
|
电子数
| 19
| 20
| 20
| 17
参考答案:D
本题解析:质子数+中子数=质量数,而质子数=核外电子数,所以选项D正确;
本题难度:简单
3、选择题 短周期主族元素X、Y、Z、W的原子序数依次增大,已知X、Y、Z+、W各微粒最外层电子数与其电子层数之比值依次为2、3、4、2,下列有关这四种元素叙述正确的是(?)
A.Y与X、Z、W分别能形成两种化合物
B.Z与W形成的Z2W型化合物在水溶液中Z+离子与W2-离子个数比为2:1
C.Y、Z、W不可能形成水溶液呈碱性的化合物
D.化合物X Y2、X YW、X W2随着共价键的键长逐渐增大,熔沸点逐渐降低
参考答案:A
本题解析:X、Y、Z+、W各微粒最外层电子数与其电子层数之比值依次为2、3、4、2,则短周期主族元素X、Y、Z、W分别是C、O、Na、S。A正确,化合物分别为H2O和H2O2、Na2S和Na2S2、SO3和SO2。B不正确,因为硫化钠溶于水,硫离子水解,在水溶液中Z+离子与W2-离子个数比大于2:1。C不正确,例如Na2SO3溶于水显碱性。D不正确,CO2是气体,而CS2是液体,答案选A。
本题难度:一般
4、填空题 (9分)短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中灼烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F,溶液F在空气中长期放置发生反应,生成物之一为H,H与过氧化钠的结构和化学性质相似,其溶液显黄色。请回答下列问题:
(1)A原子的原子结构示意图是?。
(2)B与氢氧化钠溶液反应的离子方程式是________________。
(3)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为?,当生成2mol二氧化氯时,转移电子?mol。
(4)溶液F在空气中长期放置生成H的化学方程式为?
?。
(5)H的溶液与稀硫酸反应产生的现象是?。
参考答案:(9分)(1)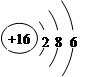 (2)2Al+2OH?+2H2O=2AlO (2)2Al+2OH?+2H2O=2AlO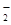 +3H2↑? +3H2↑?
(3)Na2SO4(或硫酸钠)? 2
(4)4Na2S+O2+2H2O=4NaOH+2Na2S2或
2Na2S+O2+2H2O=4NaOH+2S、Na2S+S=Na2S2
(5)溶液由黄色变为无色,产生淡黄色沉淀和(臭鸡蛋气味的)气体
本题解析:D既能溶于强酸,也能溶于强碱,则D是氢氧化铝,所以B是Al。G在大气中能导致酸雨的形成,说明G是SO2,所以E是H2S,则A是S。H2S和足量的氢氧化钠溶液反应生成硫化钠,即F是Na2S。H与过氧化钠的结构和化学性质相似,所以H应该是Na2S2。
(1)硫的原子序数是16,所以原子结构示意图为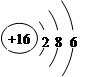
(2)铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,方程式为2Al+2OH?+2H2O=2AlO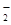 +3H2↑ +3H2↑
(3)SO2被氯酸钠氧化生成物是硫酸钠,即氧化产物是Na2SO4。氯元素的化合价从+5价降低到+4价,所以每生成2mol二氧化氯时,转移电子是2mol。
(4)硫化钠具有还原性,易被氧化,所以生成H的方程式为4Na2S+O2+2H2O=4NaOH+2Na2S2或2Na2S+O2+2H2O=4NaOH+2S、Na2S+S=Na2S2。
(5)H和稀硫酸的反应类似于过氧化钠和稀硫酸的反应,因此反应中生成硫酸钠、H2S和单质硫。因此实验现象是溶液由黄色变为无色,产生淡黄色沉淀和(臭鸡蛋气味的)气体。
本题难度:一般
5、选择题 据报道,重庆开县发生了天然气矿井“井喷”事件,喷出的气体主要成分是甲烷,还含有硫化氢(H2S)、氰化氢(HCN)等多种有毒气体,造成290多人中毒死亡.你认为喷出的气体是
A.一种纯净物
B.全部由无机化合物组成的混合物
C.全部由有机化合物组成的混合物
D.由无机化合物和有机化合物组成的混合物
参考答案:D
本题解析:H2S、HCN为无机物,天然气的主要成分甲烷为有机物.
本题难度:简单
|