1、选择题 下列说法中正确的是
[? ]
A.某离子被沉淀完全是指该离子在溶液中的浓度等于0
B.同一周期中的第ⅡA族和第ⅢA族元素的原子序数差一定为1或11
C.原电池中负极本身不一定参与电极反应
D.水的离子积常数Kw随外加酸(碱)浓度的改变而改变
参考答案:C
本题解析:
本题难度:一般
2、简答题 (1)已知常温下,AgBr的Ksp=4.9×10-13、AgI的Ksp=8.3×10-17.现向含有AgI的饱和溶液中:
①加入固体AgNO3,则c(I-)______(填“变大”、“变小”或“不变”,下同).
②若改加更多的AgI固体,则c(I-)______,而c(Ag+)______.
③若改加AgBr固体,则c(I-)______,而c(Ag+)______.
(2)难溶弱电解质在水溶液中既存在溶解平衡又存在电离平衡.已知Cu(OH)2?Cu2++2OH-,KSP=c(Cu2+)?[c(OH-)]2=2×l0-20.当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.某
CuSO4溶液里c(Cu2+)=0.02mol?L-1,如要生成Cu(OH)2沉淀,应调整沉淀pH使之大于______.
参考答案:(1)①加入AgNO3固体,使c(Ag+)增大,AgI溶解平衡向左移动,c(I-)减小,故答案为:变小;
②改加更多的AgI固体,仍是该温度下的饱和溶液,各离子浓度不变,故答案为:不变;不变;
③因AgBr的溶解度大于AgI的溶解度,所以改加AgBr固体时,使c(Ag+)变大,而使AgI的溶解平衡向生成AgI的方向移动,c(I-)变小,
故答案为:变小;变大;
(2)某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,则应有c(OH-)≥
本题解析:
本题难度:一般
3、填空题 (1)已知可逆反应:M(g)+N(g)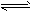 P(g)+Q(g) △H>0,请回答下列问题。
P(g)+Q(g) △H>0,请回答下列问题。
①若要增大M的转化率,在其他条件不变的情况下可以采取的措施为______(填序号)。
A.加入一定量M B.降低反应温度 C.升高反应温度
D.缩小容器体积 E.加入催化剂 F.分离出一定量P
②在某温度下起始反应物的浓度分别为:c(M)=1 mol/L,c(N)=2.4 mol/L,达到平衡后,M的转化率为
60%,此时N的转化率为_________;若保持温度不变,起始反应物的浓度改为:c(M)= 4 mol/L,c(N)=
a mol/L,达到平衡后,c(P)=2 mol/L,则a=__________mol/L。
(2)盖斯定律在生产和科学研究中有很重要的意义。试根据下列3个热化学反应方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8 kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2 kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5 kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:_____________________。
(3)一定温度下,向Na2CO3溶液中加入BaCl2和K2SO4,当两种沉淀共存时,c(CO32-):c(SO42-)=____。 [已知Ksp(BaSO4)=1.3×10-10,Ksp(BaCO3)=2.6×10-9]
参考答案:(1)①CF;②25%;6
(2)CO(g)+FeO(s)=Fe(s)+CO2(g) △H=-218.0kJ/mol
(3)20
本题解析:
本题难度:一般
4、选择题 在一定温度下,硫酸铜晶体的培养皿中存在下列平衡:Cu2+(aq)+SO42-(aq)+xH2O?CuSO4?xH2O(s),当向饱和硫酸铜溶液中加少量无水硫酸铜粉末后,下列说法中正确的是( )
A.溶液中Cu2+浓度增大
B.溶液中Cu2+数目减少
C.该硫酸铜晶体质量不变
D.溶液的蓝色变浅
参考答案:在饱和硫酸铜溶液中加入无水硫酸铜粉末,发生:CuSO4+xH2O=CuSO4?xH2O,导致溶液中水的量减少,会导致平衡:
Cu2+(aq)+SO42-(aq)+xH2O?CuSO4?xH2O(s)向正方向移动,则析出晶体后溶液仍为饱和溶液,则
A.仍为饱和溶液,则溶液中Cu2+浓度不变,故A错误;
B.Cu2+(aq)+SO42-(aq)+xH2O?CuSO4?xH2O(s)向正方向移动,溶液中Cu2+数目减少,故B正确;
C.Cu2+(aq)+SO42-(aq)+xH2O?CuSO4?xH2O(s)向正方向移动,析出晶体,硫酸铜质量增大,故C错误;
D.溶液浓度不变,则溶液颜色不变,故D错误.
故选B.
本题解析:
本题难度:简单
5、填空题 牙齿的损坏实际是牙釉质[Ca5(PO4)3OH]溶解的结果,在口腔中存在如下平衡:Ca5(PO4)3OH?5Ca2++3PO43-+OH-当糖附在牙齿上发酵时会产生H+,试运用化学平衡理论说明经常吃糖对牙齿的影响.
参考答案:牙齿的坚固部分主要成份是Ca5(PO4)3OH,糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿.其原因是在酸性条件下,H+与牙釉质溶解得到的OH-结合成水,平衡正向进行,Ca5(PO4)3OH溶解,牙釉质溶解造成龋齿;
答:糖附在牙齿上发酵时会产生H+,在酸性条件下Ca5(PO4)3OH溶解,造成龋齿.
本题解析:
本题难度:一般