1��ѡ���� ����5��7��ij��˾��ʧҿ-192����Դ���¼��ٴ�����˰�ȫ�ľ��ӡ����й���ҿ-192 ( Ir)��˵����ȷ����
Ir)��˵����ȷ����
A��ԭ������Ϊ77
B��������Ϊ115
C��������Ϊ192
D��������Ϊ77
�ο��𰸣�A
��������� Ir��ԭ������Ϊ77��������Ϊ77��������Ϊ192��������Ϊ115��
Ir��ԭ������Ϊ77��������Ϊ77��������Ϊ192��������Ϊ115��
�����Ѷȣ���
2������� X��Y��Z��W�Ƕ����ڵ�����Ԫ�أ��й����ǵ���Ϣ���±���ʾ��
Ԫ��
| ���ֽṹ֪ʶ
| ��������
|
X
| Xԭ�Ӻ������ռ��9��ԭ�ӹ��
| X��һ�����������γ��������Ҫ����
|
Y
| Yԭ�ӵĴ�������������������������һ��
| Y���γɶ�����̬�⻯��
|
Z
| Zԭ�ӵ���������������4
| ZԪ�ص���������ϼ���������ϼ۴����͵���6
|
W
| Wԭ�ӵ���������������2n-3��nΪԭ�Ӻ�����Ӳ�����
| ��ѧ��Ӧ��Wԭ����ʧȥ���������γ�Wn+
|
?
��д���пհף�����ʾ����������ĸX��Y��Z��W����
��1��X�ж���ͬ�������壬д��X2����ʽ��?��
��2��X��Y��Z����Ԫ�ص縺���ɴ�С˳��Ϊ_____��
��3��WԪ��ԭ�ӻ�̬ʱԭ�ӵĵ����Ų�ʽ_________________��
��4��Zλ��Ԫ�����ڱ���?���ڵ�?��
��5����W��һ���������dz��õľ�ˮ��������ʱ����Һ��pH?����������������������������ǣ�?�������ӷ���ʽ��ʾ����
��6��.25�桢101 kPaʱ��32 g Y����ͼ���̬�⻯����ȫȼ�������ȶ���������ʱ�ų�1780��6 kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ?��
�ο��𰸣���1��?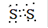 ?��2�֣�
?��2�֣�
��2��? Cl? S? C?��2�֣�
��3��1S22S22P63S23P1��2�֣�
��4����?�� ��A?����1�֣�
��5�� ��?��1�֣�? Al3++3H2O  Al(OH)3(����)��3H+��2�֣�
Al(OH)3(����)��3H+��2�֣�
CH4(g)+2O2 (g)= CO2(g)+2H2O (l) ����H =" -890.3" KJ��mol-1��3�֣�
�����������1��X�����������γ��������Ҫ���ʣ����ԭ�Ӻ�������Ų�����֪XΪS��S2������O2��ԭ�Ӽ������Ե��ӡ���2����Yԭ�ӵĽṹ��֪��ΪC����Z�Ļ��ϼۿ��ж���ΪCl�����Ե縺�ԣ�Cl>S>C����3������������������2n-3����֪��WΪAl����5��A12(SO4)3Ϊǿ�������Σ�ˮ�����Һ�����ԣ�Al3++3H2O Al(OH)3(����)+3H+����6��Y��ͼۼ����H���ʱ��������ΪCH4��32 g CH4Ϊ2 mol������1 mol CH4����-890.3kJ/mol��
Al(OH)3(����)+3H+����6��Y��ͼۼ����H���ʱ��������ΪCH4��32 g CH4Ϊ2 mol������1 mol CH4����-890.3kJ/mol��
�����Ѷȣ�һ��
3������� ��12�֣��±���Ԫ�����ڱ���һ���֣���ش��й����⣺
 | ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| 0
|
2
| ?
| ?
| ?
| ��
| ��
| ?
| ��
| ?
|
3
| ?
| ��
| ��
| ?
| ?
| ��
| ��
| ��
|
4
| ��
| ?
| ?
| ?
| ?
| ?
| ��
| ?
|
С��1:���л�ѧ��������õ�Ԫ�أ���ԭ�ӽṹʾ��ͼΪ ??��
С��2:�������γ��������������Ԫ���� ??����Ԫ�ط��ű�ʾ����д����Ԫ�صĵ����������������ˮ���ﷴӦ�Ļ�ѧ����ʽ ??��
С��3:�١��ڡ��ޡ�������Ԫ�ص�����������ˮ������������ǿ���� ?���ѧʽ����
С��4:��Ԫ�����Ԫ�����ߺ˵����֮���� ??��
С��5:���ʵ�鷽�����ȽϢ���ⵥ�������Ե�ǿ�����뽫���������±���
?
�ο��𰸣�
��1: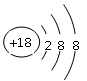 ?
?
С��2:Al��2�֣���? 2Al+ 2KOH+2H2O ="==" 2KAlO2+3H2��?��2�֣�
С��3:HClO4��2�֣�?
С��4:26?��2�֣�
С��5:��4�֣�
ʵ�鲽�裨2�֣�
ʵ����������ۣ�2�֣�
��������ˮ����ʢ���廯����Һ���Թ��У������������Ȼ�̼����
��������ˮ����Һ�ʻ�ɫ�������������Ȼ�̼�����Ȼ�̼�����ɫ��֤�������ȱȵ�����������ǿ��
�������������Ԫ�����ڱ��Ľṹ��Ԫ�������ɵ�Ӧ�á�����Ԫ�������ڱ��е�λ�ÿ��жϢ١���ֱ�ΪC��N��F��Mg��Al��S��Cl��Ar��K��Br��
С��1:����õ���ϡ������Ԫ��Ar����ԭ�ӽṹʾ��ͼΪ 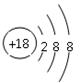 ?
?
С��2:������������������������������ܽ���ǿ�����������У���ӦʽΪ2Al+ 2KOH+2H2O ="==" 2KAlO2+3H2����
С��3:�ǽ�����Խǿ������������ˮ���������Խǿ������֪Ԫ����Cl�ķǽ�������ǿ����ۺ������������ǿ����ѧʽΪHClO4��
С��4:F��Br��ԭ�������ֱ���8��35���˵����֮����26.
С��5:�ȽϷǽ�����ǿ��ʱ����Ԫ�������ɣ�Ҳ������������������ˮ���������ǿ���������Ƿǽ������ʺ��������ϵ����׳̶��Լ���Ӧ�⻯����ȶ��ԣ������Ƿǽ���֮�����û������ȡ���˿���ͨ���������廯�Ƶ��û���Ӧ���бȽϡ�
�����Ѷȣ�һ��
4��ѡ���� ���е����У�������������������Ӧ����
A��O2
B��N2
C��F2
D��Cl2
�ο��𰸣�C
������������������ϵ����׳̶���Ԫ�صķǽ�����ǿ���йء�ͬ���ڴ�����Ԫ�صķǽ���������ǿ��ͬ������ϵ���Ԫ�صķǽ���������������F�Ƿǽ�������ǿ��Ԫ�أ�����������������Ӧ��F2�ڰ�����������������ҷ�����ը��
�����Ѷȣ�һ��
5��ѡ���� X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ��е�λ������ͼ��ʾ����Yԭ�ӵ������������Ǵ�����������3��������˵���в���ȷ����
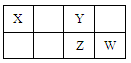
A��Y��Z�γɵĻ��������γ������ԭ��֮һ
B��W�ĵ�������ˮ��Ӧ������һ�־���Ư���Ե�����
C������������Ӧˮ��������ԣ�W >Z >X
D����̬�⻯����ȶ��ԣ�W > Z >Y
�ο��𰸣�D
�����������Ԫ�������ڱ��е�λ�ÿ�֪:Y��O��X��C��Z��S��W��Cl.A��O��S�γɵĻ�����SO2�������ԭ��֮һ����ȷ��B.������ˮ������ӦCl2��H2O HCl��HClO��������HClO��ǿ�����ԣ���һ�־���Ư���Ե����ʡ���ȷ��C��Ԫ�صķǽ�����Cl>S>C.Ԫ�صķǽ�����Խǿ��������������Ӧ��ˮ��������Ծ�Խǿ����������������Ӧˮ��������ԣ�HClO4>H2SO4 >H2CO3����ȷ��D��Ԫ�صķǽ�����O>Cl>S. Ԫ�صķǽ�����Խǿ������̬�⻯����ȶ��Ծ�Խǿ�������⻯����ȶ��ԣ�H2O > HCl >H2S.����
HCl��HClO��������HClO��ǿ�����ԣ���һ�־���Ư���Ե����ʡ���ȷ��C��Ԫ�صķǽ�����Cl>S>C.Ԫ�صķǽ�����Խǿ��������������Ӧ��ˮ��������Ծ�Խǿ����������������Ӧˮ��������ԣ�HClO4>H2SO4 >H2CO3����ȷ��D��Ԫ�صķǽ�����O>Cl>S. Ԫ�صķǽ�����Խǿ������̬�⻯����ȶ��Ծ�Խǿ�������⻯����ȶ��ԣ�H2O > HCl >H2S.����
�����Ѷȣ�һ��