1、选择题 将SO2通入BaCl2溶液至饱和,未见沉淀生成,继续通入另一种气体,仍无沉淀,则通入的气体可能是
[? ]
A.H2S
B.NaOH
C.CO2
D.Cl2
参考答案:C
本题解析:
本题难度:简单
2、选择题 下列关于氯的说法正确的是 ?(?)
?(?)
A.Cl2能使鲜花褪色是因为Cl2具有漂白性
B.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
C.氯水见光易分解,所以氯水应放在棕色瓶中避光保存
D.实验室可以用MnO2与稀盐酸反应制备Cl2
参考答案:C
本题解析:Cl2使鲜花褪色是因为Cl2与鲜花中的水反应生成的HClO具有漂白性;氯气与氢氧化钠溶液反应时氯气既做氧化剂又做还原剂;MnO2与稀盐酸不反应,所以制备Cl2应用浓盐酸。
本题难度:简单
3、填空题 请回答下列实验室中制取气体的有关问题。
(1)如图是用KMnO4与浓盐酸反应制取适量氯气的简易装置。
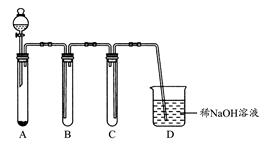
装置B,C,D的作用分别是:B?;C?;D?。
(2)在实验室欲制取适量NO气体。
①下图中最适合完成该实验的简易装置是?(填序号);
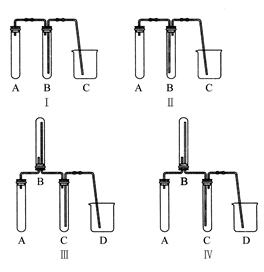
②根据所选的装置完成下表;(不需要的可不填)
?
③简单描述应观察到的实验现象?。
参考答案:(1)向上排气收集氯气 安全作用,防止D中的液体倒吸进入集气管B中 吸收尾气,防止氯气扩散到空气中污染环境
(2)①Ⅰ
②
?
应加入的物质
所起的作用
A
铜屑和稀硝酸
发生NO气体
B
水
排水收集NO气体
C
?
主要是接收B中排出的水
D
?
?
?
③反应开始时,A中铜表面出现无色小气泡,反应速率逐渐加快 A管上部空间由无色逐渐变为浅棕红色,随反应的进行又逐渐变为无色 A中的液体由无色变为浅蓝色 B中的水面逐渐下降,B管中的水逐渐流入烧杯C中
本题解析:(1)因氯气的密度比空气大,所以收集氯气时可用向上排空气法,装置B中导管是长进短出,装置C中导管是短进长出,则B,C装置能用于收集氯气的只能是装置B。装置D中盛有的稀NaOH溶液,能够吸收Cl2及挥发出的HCl。(2)实验室中可用铜与稀硝酸制取NO,因NO极易被氧化,所以收集NO不能用排空气法,应用排水法收集,可选用图I作制取NO气体的简易装置。A为NO的发生装置,加入的物质为铜屑和稀硝酸;B为排水法收集NO气体的装置,加入的物质为水;C主要是接收B中排出的水。
本题难度:简单
4、填空题 2011年“探险队员”――盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
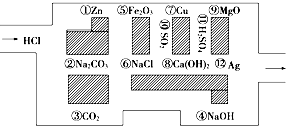
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线)___________________________________________________________________。
(2)在能“吃掉”盐酸的化学反应中,属于酸碱中和反应的有________个,属于氧化还原反应的有________个,其中能“吃掉”盐酸的盐是______________。
(3)如果将盐酸换成氯气,它能沿着盐酸走出的路线“走出”这个迷宫吗?为什么?
____________________________________________________________________。
参考答案:(1)③⑥⑩⑦1112
(2)2 1 Na2CO3
(3)否。因为氯气会与铜、氢氧化钠、氢氧化钙反应从而被“吃掉”
本题解析:(1)根据物质能否与盐酸的反应可以得出走出迷宫的路线是③⑥⑩⑦⑾⑿
(2)酸与碱的反应生成盐和水的反应称为中和反应,属于碱的有⑧和④,所以中和反应有2个。锌与盐酸的反应是氧化还原反应,所以氧化还原反应只有1个。能与盐酸反应的盐是碳酸钠。
(3)若将盐酸换位氯气,氯气会与铜、氢氧化钙、氢氧化钠反应恰好将道路堵住所以不能通过。
本题难度:一般
5、选择题 某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液(已知氯气和NaOH在一定温度下能发生反应:3Cl2+6NaOH=5NaCl+NaClO3+3H2O),经测定ClO-与ClO3-的物质的量之比为1:3,则氯气与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( )
A.21:5
B.11:3
C.3:1
D.4:1
参考答案:根据ClO-与ClO3-的浓度之比1:3,由Cl到ClO-,失去1个电子,由Cl到ClO3-,失去5个电子,一共失去1+3×5=16个电子;由Cl到Cl-,得到1个电子,需要16个原子才能得到16个电子,所以,被还原的氯元素与被氧化的氯元素的物质的量之比=16:(1+3)=4:1.
故选:D.
本题解析:
本题难度:一般