1��ѡ���� ����ˮ��������������ijѧ������������ˮȥ��������������Һ����������Ե�ҩƷ�����������
[? ]
A��NaNO3
B��FeCl2
C��NaHSO3
D��AlCl3
�ο��𰸣�BC
���������
�����Ѷȣ���
2��ѡ���� ��������ˮ�Dz������������ģ�Ϊ��������ˮ��Cl�C�Ĵ��ڣ����ѡ�����������е� (? )
A��ʯ����Һ
B�����Ȼ�̼
C������������Һ
D����������Һ
�ο��𰸣�D
���������������������Һ�����ְ�ɫ���������ǣ�˵����Cl�C�Ĵ��ڣ���D��ȷ��
�����Ѷȣ���
3������� �������ȣ�ClO2����һ����ˮ�����ȷ����й㷺Ӧ�õĸ�Ч��ȫ����������Cl2���á�
��?��ClO2���Ʊ������У������������Ʊ������� ?
����һ��2NaClO3��4HCl=2ClO2����Cl2����2NaCl��2H2O ?
��������2NaClO3��H2O2��H2SO4=2ClO2����Na2SO4��O2����2H2O ?
�÷������Ʊ���ClO2���ʺ���������ˮ����������Ҫԭ����____________?��
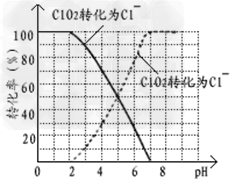
��?��ClO2������������ˮ��pH?5.5��6.5��������һ���������岻��������������ӣ�ClO2-��������ˮ�е�ClO2��ClO2-���������������������вⶨ��ClO2��I-��ԭΪClO2-��Cl-��ת��������ҺpH�Ĺ�ϵ����ͼ��ʾ����pH��2?.0ʱ��ClO2-Ҳ�ܱ�I-��ȫ��ԭΪCl-����Ӧ���ɵ�I2�ñ�Na2S2O3��Һ�ζ���2Na2S2O3+?I2=?Na2S4O6?+?2NaI
����д��pH��2?.0ʱClO2-��I-��Ӧ�����ӷ���ʽ______________��
���������Ӧ��ʵ�鲽�裺
����1��ȷ��ȡV?mLˮ�����뵽��ƿ�С�
����2������ˮ����pHΪ7.0��8.0��
����3������������KI���塣
����4��?��������������Һ����c?mol��L��1Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��ҺV1mL��
����5��_______________________��
����6������c?mol��L-1Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��ҺV2?mL��
�۸��������������ݣ���ø�����ˮ��ClO2-��Ũ��Ϊ___________mol��L��1���ú���ĸ�Ĵ���ʽ��ʾ����
�ο��𰸣��ŷ������Ʊ���ClO2
�Ƣ�ClO2-+4H++4I-=Cl-+2I2+2H2O���ڵ�����Һ��pH��2.0�� ��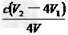
���������
�����Ѷȣ�һ��
4��ʵ���� ��12�֣�Ϊ�о��¶ȶ�Cl2��KOH��Ӧ��Ӱ�죬���ʵ�����£�
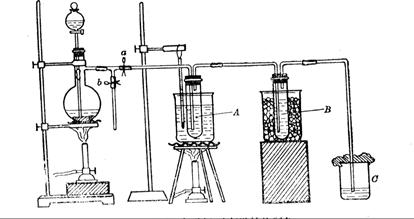
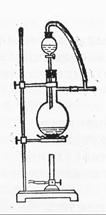
��������ƿ��װ������MnO2����Һ©����װ����Ũ���ᣬ���Թ�A��װ4mol/LKOH��Һ15mL��������75��ˮԡ�У����Թ�B��װ02mol/LKOH��Һ�������ڱ�ˮ�У�C��װNaOH��Һ��
�Իش��������⣺
��1��ˮԡ������ʲô�ŵ㣿
��2������ж�A���Ѿ���Ӧ��ȫ��
��3������A�����ɵ������Σ���ⷢ������KClΪ005mol��������HCl�ӷ�����д��A�з����Ļ�ѧ����ʽ
��4������B�����ɵ������Σ� �����ʵ���֮��Ϊ1��1��д�����ӷ���ʽ��
�����ʵ���֮��Ϊ1��1��д�����ӷ���ʽ��
��5���Թ�BҪ���ڱ�ˮ�н��µ���Ҫԭ���ǣ�
A�����Թ�A�г����������¶Ƚϸߣ���ʹ�Թ�B�е���Һ�¶�����
B����ֹ���ɵ��ηֽ�
C����������ˮ�л�����ǿ
D���÷�Ӧ�Ƿ��ȷ�Ӧ��Ϊ��ֹ�¶ȹ��ߣ����ý���
 ������ͼ�������𣿡�
������ͼ�������𣿡�