1������� ��17�֣�Na��Cu��Al��O��C��H�dz���������Ԫ�ء�
��1��Alλ��Ԫ�����ڱ���_____���ڵ�_____�壻Cu�Ļ�̬ԭ�Ӽ۵����Ų�ʽΪ__________��
��2���á�����������գ�
��һ������
| ���Ӱ뾶
| �е�
|
Na_______Al
| O2��_______Na+
| CH4______H2O
|
��3��250��ʱ�������Ͻ�Ϊ��������4 L������ͨ��6 mol CO2��6 mol CH4���������·�Ӧ��CO2 (g)��CH4(g)  2CO(g)��2H2(g)��ƽ����ϵ�и��������������±���
2CO(g)��2H2(g)��ƽ����ϵ�и��������������±���
�� ��
| CH4
| CO2
| CO
| H2
|
�������
| 0.1
| 0.1
| 0.4
| 0.4
|
�ٴ��¶��¸÷�Ӧ��ƽ�ⳣ��K=__________
����֪��CH4(g)��2O2(g)��CO2(g)��2H2O(g) ��H=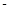 890.3 kJ��mol��1
890.3 kJ��mol��1
CO(g)��H2O (g)��CO2(g)��H2 (g) ��H="+2.8" kJ��mol��1
2CO(g)��O2(g)��2CO2(g) ��H=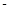 566.0 kJ��mol��1
566.0 kJ��mol��1
��ӦCO2(g)��CH4(g) 2CO(g)��2H2(g) �ġ�H=________________
2CO(g)��2H2(g) �ġ�H=________________
��4���Զ������ѱ��渲��Cu2Al2O4Ϊ���������Խ�CO2��CH4ֱ��ת�������ᡣ
���ڲ�ͬ�¶��´����Ĵ�Ч���������������������ͼ��ʾ��250��300��ʱ���¶����߶�������������ʽ��͵�ԭ����_____________________.

��Ϊ����߸÷�Ӧ��CH4��ת���ʣ����Բ�ȡ�Ĵ�ʩ��__________________
��5�����ø��µ�⼼���ɽ��ͷŵ�CO2ת��Ϊ���й�ҵ���ü�ֵ�IJ�Ʒ��
��Ӧ����ʽΪ�� ���乤��ԭ��ʾ��ͼ���£�
���乤��ԭ��ʾ��ͼ���£�

CO2�ڵ缫a�ŵ�ķ�Ӧʽ��_______________________________
2������� ��������ʵ�У�ʲô����Ӱ���˻�ѧ��Ӧ�����ʣ�?
��1������ƿ����H2��Cl2�Ļ�����壬��ƿ���ȼþ��ʱ������ը______________��
��2������������ʱҪ�����ϸС�Ŀ���__________________��
��3��KI�����HgCl2�����Ϻ�������������һ��Ͷ��ˮ�У��ܿ����ɺ�ɫHgI2________________��
��4���ۻ���KClO3�ų����ݺ�������������MnO2�ܿ��������__________________��
��5��ͬŨ�ȡ�ͬ����������з���ͬ����С��п����þ�飬���������п�����__________________��
��6��ͬ����С��ʯ��ʯ�ֱ���0��1mol/L�������1mol/L�������з�Ӧ���ʲ�ͬ_______________��
��7�������ʳƷ�ױ�ù������Ͳ�����������__________________��
3������� �����ӡ�ʵ���У�3I- +S2O82- =I3-+ 2SO42-�ķ�Ӧ���ʿ�����I3-�����ĵ�����Һ����ɫ��ʱ��t��������tԽС����Ӧ����Խ��ij̽����ѧϰС����20�����ʵ�飬�õ����������±����ش��������⣺
(1)��ʵ���Ŀ����____________��
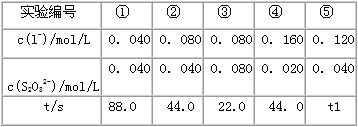
(2)��ɫʱ��t1=_____________��
(3)�¶ȶԸ÷�Ӧ�ķ�Ӧ���ʵ�Ӱ�����һ����ɣ�����40���½��б�Ţ۶�ӦŨ�ȵ�ʵ�飬��ɫʱ��
t2 �ķ�ΧΪ__________������ĸ����
A��<22��0s B��22��0��44��0s C��>44��0s D�����ݲ��㣬���ж�
(4)ͨ�������Ƚ��ϱ����ݣ��õ��Ľ�����__________________��
4������� �Ͼ�ӡˢ��·��Ļ������ÿ�ʵ����Դ��������������Ⱦ���Ͼ�ӡˢ��·�徭������룬�ܵõ��ǽ�����ĩ�ͽ�����ĩ��
��1�����д���ӡˢ��·��ǽ�����ĩ�ķ����У������ϻ��������������______________��
A�����ѽ��γ�ȼ�� B��¶����� C����Ϊ�л����Ͻ������ϵ�ԭ�� D��ֱ������
��2����H2O2��H2SO4�Ļ����Һ���ܳ�ӡˢ��·�������ĩ�е�ͭ����֪��
Cu(s)��2H+(aq)=Cu2+(aq)��H2(g) ��H=64��39kJ��mol-1
2H2O2(l)=2H2O(l)��O2(g) ��H=��196��46kJ��mol-1
H2(g)��1/2O2(g)=H2O(l) ��H=��285��84kJ��mol-1
��H2SO4��Һ��Cu��H2O2��Ӧ����Cu2+��H2O���Ȼ�ѧ����ʽΪ_______________________��
��3����������������ͬ��ӡˢ��·��Ľ�����ĩ��10�GH2O2��3��0mol��L-1 H2SO4�Ļ����Һ��������ò�ͬ�¶���ͭ��ƽ���ܽ�����(���±�)��
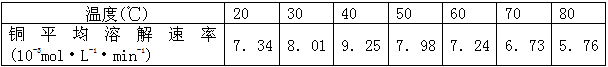
���¶ȸ���40��ʱ��ͭ��ƽ���ܽ��������ŷ�Ӧ�¶����߶��½�������Ҫԭ����________________________________________________________________��
��4�����ᴿ���CuSO4��Һ�м���һ������Na2SO3��NaCl��Һ�����ȣ�����CuCl�������Ʊ�CuCl�����ӷ���ʽ��____________________________��
5������� ��һ���¶��£���һ���ݻ�Ϊ2L���ܱ������У���������������������·�Ӧ��
2SO2(g)+O2(g) 2SO3(g) ����H����196.6kJ��mol-1 �ڷ�Ӧ������10min��20minʱ���ı���Ӱ�췴Ӧ��һ����������Ӧ������ͼ��ʾ��
2SO3(g) ����H����196.6kJ��mol-1 �ڷ�Ӧ������10min��20minʱ���ı���Ӱ�췴Ӧ��һ����������Ӧ������ͼ��ʾ��

��1��ǰ10min����Ӧ���ʱ仯������_____________��������С�䣩ǰ15minƽ����Ӧ������SO3Ũ�ȱ仯�ɱ�ʾΪ��____________________��
��2������ͼ��ʾ�ķ�Ӧ�����У���ʾ����Ӧ�������淴Ӧ������ȵ�ʱ�����________________��
��3����ͼ�жϣ�10minʱ�ı�ķ�Ӧ����������____________����д��ţ���ͬ���� 20minʱ�ı�ķ�Ӧ����������____________��
a.���˴��� b.��С������� c.�����¶� d.����O2�����ʵ���