1������� ��ͼ��ʵ������ȡ���ռ�Cl2��װ�ã�A��Cl2����װ�ã�E��Ӳ�ʲ�������װ��ϸ��˿����FΪ����Ĺ��ƿ���ձ�GΪβ������װ�ã�
�Իش�
��1��A�з����Ļ�ѧ��Ӧ����ʽΪ______��
��2��C��D��G�и�װ��ҩƷ��C______��D______��G______��
��3��E�е�����Ϊ______����Ӧ����ʽΪ______��
��4��д��G�з�Ӧ�����ӷ���ʽ______��
��5������Cl2��SO2�����ʵ������Ư�����ü������û�ѧ����ʽ����ԭ��______��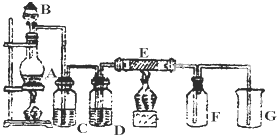
�ο��𰸣���1��A����ʵ�����������ķ���װ�ã������Ļ�ѧ��Ӧ����ʽΪ��MnO2+4HCl��Ũ��?��?.?MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4HCl��Ũ��?��?.?MnCl2+Cl2��+2H2O��
��2��ʵ���Ʊ������к����������Ȼ����ˮ������ͨ��Eװ��ʱ��Ҫ��ȥ���ʣ�����ͨ������ʳ��ˮ��ȥ�Ȼ��⣬ͨ��Ũ�����ȥˮ�����������ж������ŵ������У�Ҫ����β�����գ��ʴ�Ϊ������NaCl��Һ��ŨH2SO4 ��NaOH��Һ��
��3������������Ӧ�����Ȼ��������غ�ɫ�̣����ҷ�Ӧ���ȣ��÷�ӦΪ2Fe+3Cl2?��ȼ?.?2FeCl3 ��
�ʴ�Ϊ�����ҷ�Ӧ�������غ�ɫ���غ�ɫ�����̣��ų������ȣ�2Fe+3Cl2?��ȼ?.?2FeCl3 ��
��4��G�з�Ӧ��β������װ�ã������ж���Ҫ������������Һ���գ���Ӧ�����ӷ���ʽΪ��Cl2+2OH-�TCl-+ClO-+H2O���ʴ�Ϊ��Cl2+2OH-�TCl-+ClO-+H2O��
��5������Cl2��SO2�����ʵ������Ư�����ü������������������ԣ�����������л�ԭ�ԣ�����1��1����������ԭ��Ӧ������������ᣬ��Ӧ�Ļ�ѧ����ʽΪ��Cl2+SO 2+2H2O�TH2SO4+2HCl���ʴ�Ϊ��Cl2+SO 2+2H2O�TH2SO4+2HCl��
���������
�����Ѷȣ�һ��
2��ѡ���� ʵ���ҽ�������ʵ��ʱ��Ҫ�õ��¶ȼƣ����¶ȼ�ˮ�������ڷ�Ӧ��Һ�����µ��ǣ�������
A���������ᴿˮ
B����ȩ��������Ӧ
C��ʵ��������ϩ
D��ʵ������ȡ������
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� ʵ���ҿ��ö������̷�ĩ��Ũ���Ṳ����ȡ��������ֻ��Ũ���ᣬ��û�ж������̣����и����Լ��У������������������ȡ��������
[? ]
A��KMnO4
B��KClO3
C��CaCl2
D��Ca(ClO)2
�ο��𰸣�C
���������
�����Ѷȣ���
4������� ʵ������������������̻�ϼ����Ʊ�Cl2��ͬʱ����MnCl2��H2O���˷�Ӧ�Ļ�ѧ����ʽΪ____�� �����ӷ���ʽΪ___������������Ϊ ___����ԭ��Ϊ___������___���ռ�Cl2��
�ο��𰸣�MnO2 +4HCl(Ũ) MnCl2+Cl2��+2H2O ��MnO2+4H++ 2Cl-
MnCl2+Cl2��+2H2O ��MnO2+4H++ 2Cl- Mn2++Cl2��+2H2O ��
Mn2++Cl2��+2H2O ��
MnO2 ��HCl �������ſ���
���������
�����Ѷȣ�һ��
5������� ʵ������Ũ��������250mL0.1mol/L��������Һ����
��1������250mL0.1mol/L������Һ��ҪŨ���ᣨ�ܶ�Ϊ1.2g/mL����������Ϊ36.5%�������Ϊ______��
��2������ʱ������ȷ�IJ���˳���ǣ���ĸ��ʾ��ÿ����ĸֻ����һ�Σ�______��
A����30mLˮϴ���ձ�2-3�Σ�ϴ��Һ��ע������ƿ����
B������Ͳ��ȡ�����Ũ���ᣬ�ز����������ձ��У��ټ�������ˮ��Լ30mL�����ò���������������ʹ���Ͼ���
C��������ȴ�������ز�����ע��250mL������ƿ��
D��������ƿ�ǽ�����ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ����ǡ����̶�����
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1-2cm��
��3���������ʵ���Ũ�ȵ���Һ�����Ũ��ƫ�ߵIJ�����______��
A���ܽ�����Һδ�������¾�ת������ƿ�У�
B��ϴ���ձ��Ͳ�������Һδת������ƿ�У�
C������ʱ�۾����ӿ̶��ߣ�
D������ʱ�۾����ӿ̶��ߣ�
��1��ijѧ����Ƶ��ø�Ũ������������̷�Ӧ��ȡ���ռ����﴿����������װ����ͼ��
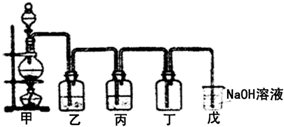
��д�����з�����Ӧ�����ӷ���ʽ��______
������ʢ���Լ���______��������______��
����ʢ���Լ���______��
��2���������������������20mL��Ũ�����ϼ��ȣ���ַ�Ӧ�������Ͽ����ɱ���µ����������Ϊ______mL����ʵ��ֵ������������ֵ������Ҫԭ���У�
��______����______��
��3�������Ƶõ���������ͨ����ɫ�ı��͵⻯����Һ�У���Һ��______ɫ�������ӷ���ʽ��______����������Һ�м������Ȼ�̼�����ã�����Һ��Ϊ���㣬�²�����______ɫ�����ֲ�������______��
��4�������Ƶõ������Ƴɱ�����ˮ����ʵ���ұ��汥����ˮ�ķ�����______��
�ο��𰸣���1����Ũ��������ʵ���Ũ��c=1000��1.2��36.5%36.5mol/L=12.0mol/L������ϡ�Ͷ��ɣ�ϡ��ǰ�����ʵ����ʵ������䣬������Ũ������������Ũ��������ΪxmL������xmL��12.0mol/L=250mL��0.1mol/L����ã�x��2.1��
����Ũ��������Ϊ2.1mL��
�ʴ�Ϊ��2.1mL��
��2�����������м��㡢��ȡ��ϡ�͡���Һ��ϴ����Һ�����ݡ�ҡ�ȵȲ���������Ͳ��ȡ���õ���ͷ�ιܣ�Ũ���ᣬ���ձ���ϡ�ͣ��ò��������裬�ָ����º�ת�Ƶ�250mL����ƿ�У����ò�����������ϴ��2-3�Σ���ϴ��Һת�Ƶ�����ƿ�У���ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμӣ�����ݵߵ�ҡ�ȣ�
���Բ���˳����BCAFED��
�ʴ�Ϊ��BCAFED��
��3��A����Һ�����������������ʣ�δ��ȴ�����£����Ƚ���Һ��������ƿ���������Һ���ᵼ����Һ���ƫС����ҺŨ��ƫ�ߣ�
B��ϴ��Һ�к��������Ȼ��⣬��������ƿ�������Ȼ�������ʵ�����С��������ҺŨ��ƫ�ͣ�
C������ʱ���ӿ̶��ߣ�������Һ�����С��������ҺŨ��ƫ�ߣ�
D������ʱ���ӿ̶��ߣ�������Һ�������������ҺŨ��ƫ�ͣ�
��ѡ��AC��
��1��ʵ�����õ�һ��װ���Ʊ���������Ӧ���ӷ���ʽΪMnO2+4H++2Cl-=Mn2++Cl2��+2H2O����HCl��H2O�Ļӷ����ݳ��������г����������Ȼ����ˮ�����������ռ��������������������Ӧ���о�����������ͨ��ʢ�б���ʳ��ˮ��Ũ�����ϴ��ƿ��ʹ�Ȼ����ܽ��ڱ���ʳ��ˮ�������ڱ���ʳ��ˮ���ܽ�ȴ�ͣ���ˮ������Ũ�������գ��������ľ��������������ͽϴ����ˣ������ж�������ֱ���ŷŵ������У�Ӧ��ʢ��NaOH��Һ��װ���ռ���
�ʴ�Ϊ����MnO2+4H++2Cl-=Mn2++Cl2��+2H2O
�ڱ���NaCl��Һ��?��ȥCl2�л��е�HCl���壮?ŨH2SO4��
��2��MnO2+4HCl��Ũ��?��?.?MnCl2+Cl2��+2H2O
? 4mol? 22.4L
0.02L��12.0mol/L=0.24mol? V
����V=0.24mol4mol��22.4L=1.344L=1344?mL��
�������̲�����ϡ���ᷴӦ����Ӧ�����Ȼ��⣬Ũ�����ӷ����Ȼ��ⶼ�ᵼ������Ũ�ȱ�С��
�ʴ�Ϊ��1344?mL��?�ٲ���Ũ����ӷ��ˣ������ŷ�Ӧ�Ľ���Ũ�����ϡ��ϡ����ܱ�������������
��3�����������Ժ�ǿ��������������Ϊ�ⵥ�ʣ���Ӧ���ӷ���ʽΪCl2+2I-=2Cl-+I2����ˮ���ػ�ɫ��
�������Ȼ�̼���ܽ��Զ����ˮ�У����Ȼ�̼�ܶȱ�ˮ���Ҳ�����ˮ��������Һ�ֲ㣬�²�Ϊ�Ϻ�ɫ���ò���Ϊ��ȡ��
�ʴ�Ϊ���ػƣ�Cl2+2I-=2Cl-+I2���Ϻ죻��ȡ��
��4����������������ֽ⣬������ˮӦ������ϸ����ɫ�Լ�ƿ�У������䰵����
�ʴ�Ϊ��������ϸ����ɫ�Լ�ƿ�У������䰵����
���������
�����Ѷȣ�һ��