1、实验题 某研究性学习小组利用如图所示装置完成有关实验。
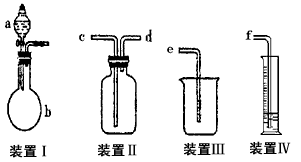
【实验一】快速制氨气
(1)用装置I快速制氨气,则装置I的a仪器中可加入浓氨水,b仪器中加入________。装置Ⅱ从_____管口进气可作为氨气的收集装置。实验过程中,使用分液漏斗滴加液体的操作是________________。
(2)该实验剩余的NH3需吸收处理。以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有
________
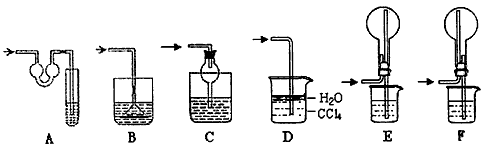
(3)实验中若需用所给装置量取NH3的体积,试简述操作方法____________________所装液体最好是
____(填字母编号)
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
本实验应对量气装置多次读数,读数时应注意:①将实验装置恢复到室温,②________________,③视线与凹液面最低处相平。
【实验二】比较盐酸、碳酸、硅酸的酸性强弱(可以不填满,也可以再加行)
(4)用所给装置设计实验,完成下列表格

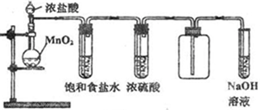
2、实验题 某校化学兴趣小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如图所示:

(1)写出该反应的化学方程式__________________。
(2)上述反应中,还原剂是______,1 mol该还原剂被氧化时转移的电子的物质的量是____mol。
(3)实验开始前,某学生对装置进行了气密性检查。方法是:连接好装置后,用弹簧夹夹住____(填“A”或“B”)处橡胶管,向分液漏斗中加水并打开活塞,当加到一定量时,停止加水,静置观察,当观察到分液漏斗中____ 时,表明该装置不漏气。
(4)兴趣小组的某些同学准备在烧杯中加入下列溶液中的一种来吸收残余氯气,你认为错误的是____(填字母)。
A.氢氧化钠溶液 B.碳酸钠浓溶液 C.浓H2SO4
3、简答题 如图1是某研究性学习小组利用实验室制氯气的装置设计制取氯水并进行相关实验.

(1)A装置中发生化学反应的离子方程式为______.
(2)氯气能使湿润的红色布条褪色.对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能.请你设计实验,得出正确结论.
①提出假设假设一______.假设二______.假设三______.假设四H2O使布条褪色
②设计实验方案
基于提出的假设,设计出实验方案(不需要作答)
③实验过程
实验①:______;实验②:______.实验③:把红色布条放在水里,布条不褪色.
④得出结论______.
(3)用量筒取20mL氯水,倒入已检查完好的分液漏斗中,然后再注入10mLCCl4,盖好玻璃塞,振荡,静置于铁架台上(如图2),等分层后取上层液和下层液,呈黄绿色的是______(填“上层液”或“下液”),再装入如图3所示的烧杯中,能使有色布条褪色的是______(填“上层液”或“下层液”)
(4)上述制备并吸收氯气装置的缺点是______,如何改进______,在图4框中画出改进的实验装置图______.
4、填空题 实验室可以用二氧化锰和浓盐酸反应制取氯气,方程式如下:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,图是某学生设计的试验室制备干燥Cl2的试验装置图,根据图中的装置和有关试剂回答下列问题.
(1)该试验还缺少一种仪器,这种仪器是______;
如果反应正常进行,回答下列问题:
(2)收集到的氯气颜色为______,密度比空气______;
(3)下列溶液的作用是:
①饱和食盐水______.
②浓硫酸______.
③NaOH溶液______.
(4)写出Cl2和NaOH溶液反应的离子方程式______.
5、简答题 Cl2的实验室制取与性质验证是高中化学实验的基础实验之一,结合所给装置图Ⅰ、Ⅱ、Ⅲ,回答下列问题.
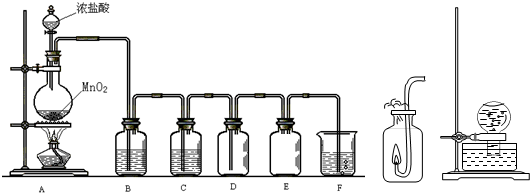
(1)在制取有毒气体时,通常使用“制备→净化→干燥→收集→尾气处理”五部分装置.在图Ⅰ中E、F属于尾气处理装置,其中E的作用是______.
(2)写出图Ⅰ圆底烧瓶中发生反应的化学方程式______;在F所指的装置中,通常盛放的试剂为______,写出该装置中发生的离子反应方程式______.
(3)请你结合图Ⅱ,描述该实验的实验现象______.
(4)将装有饱和氯水的烧瓶,倒置于水槽中,放置在阳光直射处,如图Ⅲ所示.一段时间后,可以观察有气泡产生,该反应的化学方程式为______.
(5)用高锰酸钾和浓盐酸在室温下就能很快制得氯气,由此可以比较二氧化锰和高锰酸钾中氧化性较强的是______.