1������� ��ͭƬ��пƬ��200mL?ϡH2SO4��ɵ�ԭ����У���пƬֻ�����绯ѧ��Ӧ����ͭƬ�Ϲ��ų�3.36L����״��������ʱ��H2SO4ǡ����ȫ���ģ���
��1����Ӧ�����ĵ�п�������Ƕ��٣���Zn��65��
��2���ж��ٸ�����ͨ���˵��ߣ�
��3��ԭϡH2SO4�����ʵ���Ũ���Ƕ��٣�
�ο��𰸣���1������п��ͭ���ã�����п���������������ĵĽ���Ϊп��
пʧ��������п���ӽ�����Һ���缫��ӦʽΪпƬ��Zn-2e-=Zn 2+��ͭƬ�������ӵõ����������������Ե缫��ӦʽΪ��ͭƬ��2H++2e-=H2����
�ܷ�Ӧ��Zn+2H+=H2��+Zn 2+
? 65g? 22.4L
? 9.75g? 3.36L
�������Ľ���������Ϊ9.75g��
�ʴ�Ϊ9.75g��
��2��Zn+2H+=H2��+Zn2+ת�Ƶ���
? 22.4L? 2mol
? 3.36L? 0.3mol
����ת�Ƶ��ӵ����ʵ���Ϊ0.3mol����1.806��1023����
�ʴ�Ϊ1.806��1023����
��3��������ԭ���غ㣬H+ȫ����H2SO4�ṩ��
����n��H2��=n��H2SO4��=0.15mol
c��H2SO4��=0.15mol?0.2L=0.75mol/L
�ʴ�Ϊ0.75mol/L��
���������
�����Ѷȣ�һ��
2������� ��ˮ���̲��ŷḻ����Դ����ˮ�ۺ����õ�����ͼ��ͼ1��
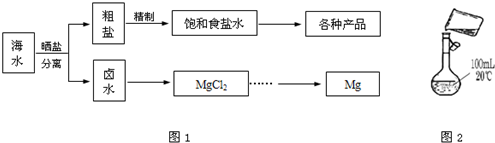
��1��Ϊ���龫�δ��ȣ�������250mL?0.2mol/L?NaCl�����Σ���Һ��ͼ2�Ǹ�ͬѧת����Һ��ʾ��ͼ��ͼ�������������ָ����______
��2����NaCl��ԭ�Ͽ��Եõ����ֲ�Ʒ��
ʵ�����ö��Ե缫���100mL?0.1mol/LNaCl��Һ���������������õ�112mL���壨��״����������������ȫ������Һ���ݳ�������������Һ��pHΪ______�����Է�Ӧǰ����Һ������仯����
��3���ȼҵ�Ǹߺ��ܲ�ҵ��һ�ֽ�������ȼ�ϵ������ϵ��¹��տ��Խڣ��磩��30%���ϣ������ֹ�������У�������ϵĴ�����ת����ϵ��ͼ3��ʾ�����еĵ缫δ��������õ�����Ĥ��ֻ����������ͨ����
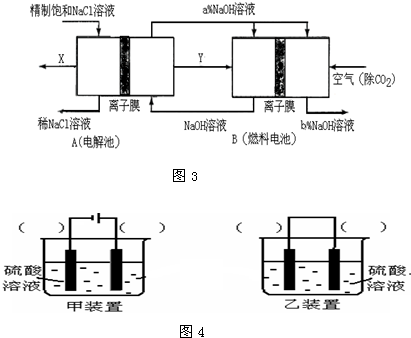
��ͼ��X��Y�ֱ���______��______���ѧʽ������д��ȼ�ϵ��B�����������ĵ缫��Ӧ______��
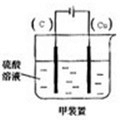
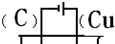
��4��ͼ4��ʵ��Cu+H2SO4�TCuSO4+H2��������Ϊ��ʵ�ָ�ת����װ���е������ڣ�����缫���ϣ��Cu����C������
�ο��𰸣���1������һ�����ʵ���Ũ�ȵ���Һʵ�飬����Һʱ��Ҫ�ò�������������ͼ��ͬѧ��ת����Һʱû���ò���������������250mL����ҺҪ����250mL������ƿ���ʴ�Ϊ��δ�ò�����������δ����250?mL����ƿ��
��2�����ⱥ��ʳ��ˮ�ķ���ʽ��2NaCl+2H2O?ͨ��?.?2NaOH+H2��+Cl2������������H2�����Ϊ112mL��0.005molʱ�������������Ƶ����ʵ���Ϊ0.01mol��������Һ��NaOH�����ʵ���Ũ��=0.01mol0.1L�T0.1mol/L�����������ӵ�Ũ��Ϊ1��10?-140.1=1��10-13mol/L��PH=13���ʴ�Ϊ��13��
��3���ٵ�ⱥ��ʳ��ˮʱ��������������ʧ�������������Ĺ��̣������������ӵõ������������Ĺ��̣��ʴ�Ϊ��Cl2��H2��
������ȼ�ϵ�صĵ�����Ǽ�ʱ������ܷ�Ӧʽ���ɱ�ʾΪ��2H2+O2=2H2O����������Ӧ��ʾΪ��O2+2H2O+4e-=4OH-���ʴ�Ϊ��O2+4e-+2H2O=4OH-��
��4��Cu��H2SO4֮��ķ�Ӧ�Ƿ��Է��ģ���Ҫ����ʵ�֣�����ͭ�������������ǵ��弴�ɣ������Ϊ���ᣬ����
���ʴ�Ϊ��
��
���������
�����Ѷȣ�һ��
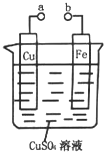
3��ѡ���� ijѧϰС��Ϊ�о��绯ѧԭ���������ͼװ�ã�������������ȷ���ǣ�������
A��a��b������ʱ����Ƭ�ϻ��н���ͭ����
B��a��b�õ�������ʱ��ͭƬ�Ϸ����ķ�ӦΪ��Cu2++2e-=Cu
C��a��b�ֱ������㹻��ѹ��ֱ����Դ��������ʱ��Cu2+��ͭ�缫�ƶ�
D������a��b�Ƿ��õ������ӣ���Ƭ���ܽ⣬��Һ����ɫ���dz��ɫ