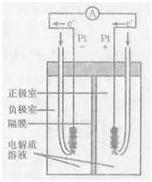
1、选择题 下列说法中不正确的是( )
A.对于吸热反应,反应物所具有的总能量低于生成物所具有的总能量
B.放热反应在常温条件下不一定能发生
C.1mol硫酸跟足量氢氧化钠发生中和反应放出的热叫做中和热
D.在?101?kPa?时,1?mol?纯物质完全燃烧生成最稳定的氧化物时所放出的热量就叫做该物质的燃烧热
2、选择题 下列反应属于氧化还原反应,且生成物的总能量高于反应物的总能量的是(?)
A.铝热反应
B.铝与盐酸反应
C.Ba(OH)2・8H2O晶体和NH4Cl晶体反应
D.灼热的炭与CO2反应
3、选择题 下列说法正确的是(?)
A.凡是放热反应的发生都不需要加热
B.凡是需要加热才能发生的反应都是吸热反应
C.凡是伴有能量变化的物质变化都一定是化学变化
D.物质发生化学反应都伴随着能量变化
4、填空题 (12分)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
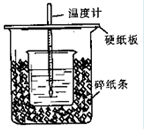
(1)从实验装置上看,图中尚缺少的一种玻璃用品是?。
(2)烧杯间填满碎纸条的作用是?。
(3)大烧杯上如不盖硬纸板,求得的中和热数值?(填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量?(填“相等、不相等”),所求中和热?(填“相等、不相等”),简述理由?。
5、填空题 以节能减排为基础的低碳经济已成为实现人类可持续发展的重要课题。
(1)控制和治理CO2是解决温室效应的有效途径,其中一种途径是将CO2转化成有机物实现碳循环。如2CO2(g)+2H2O(1)?C2H4(g)+3O2(g)△H=+1411.0kJ/mol
2CO2(g)+3H2O(1)?C2H5OH(1)+3O2(g)△H=+1366.8kJ/mol
则由C2H5OH(1)转化为C2H4(g)和H2O(1)的热化学方程式为?。
(2)为探究反应6H2(g)+2CO2(g)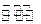 CH3CH2OH(g)+3H2O(g)发生的适宜条件,现改变氢碳比[n(H2)/n(CO2)]和温度等条件进行了如下实验:
CH3CH2OH(g)+3H2O(g)发生的适宜条件,现改变氢碳比[n(H2)/n(CO2)]和温度等条件进行了如下实验:
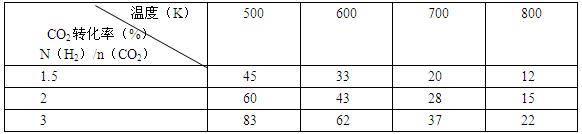
根据表中实验数据分析:
①该反应的正反应为?(填“吸热”或“放热”)反应。
②为提高CO2的平衡转化率,可采取的措施有?(写出一条即可)。
(3)一定条件下,将3 mol H2和1mol CO2气态混合物充入2L密闭容器中,发生如下反应:3H2(g)+CO2(g)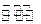 CH3OH(g)+H2O(g)。2min时该反应达到平衡,测得CH3OH的物质的量浓度为0.2mol/L。下列说法正确的是?。
CH3OH(g)+H2O(g)。2min时该反应达到平衡,测得CH3OH的物质的量浓度为0.2mol/L。下列说法正确的是?。
A.该反应的平衡常数表达式为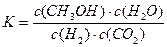
B.CO2的平衡转化率为40%
C.2min内H2的平均反应速率为0.3mol/(L・min)
D.该反应达到平衡状态的标志是混合气体的密度不发生改变