1、选择题 主族元素的化学性质主要取决于
A.元素的化合价
B.原子的质量数
C.原子的最外层电子数
D.原子半径
参考答案:C
本题解析:主族元素的化学性质主要取决于原子的最外层电子数,即价电子数,答案选C。
点评:该题是基础性试题的考查,难度不大。主要是考查学生对原子结构和元素化学性质关系的了解掌握情况,旨在巩固基础,提高学生的应试能力。
本题难度:简单
2、填空题 (8分)填写下列空白(填序号):
①CH4 ②CH2==CH2 ③CH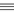 CH?④NH3 ⑤NH4+⑥BF3 ⑦P4
CH?④NH3 ⑤NH4+⑥BF3 ⑦P4
⑧H2O ?⑨H2O2?⑩ SO2?⑾PCl3?⑿SO3?⒀HCHO?⒁CO2
(1) 呈正四面体的是________。
(2) 属于极性分子且中心原子轨道为sp3杂化的是__________________________,
属于非极性分子且中心原子轨道为sp2杂化的是___________,为sp杂化的是________。
(3) 所有原子共平面的是______________,共线的是______________。
(4) 微粒存在配位键的是________。(5)含有极性键的极性分子是________。
参考答案:(1)、①⑤⑦ (2)、①④⑧⑨⑾ ?②⑥⑿ ③⒁
(3)、②③⑥⑧⑩⑿⒀⒁ ③⒁ (4)、⑤ (5)④⑧⑨⑩⑾⒀
本题解析:
(1)、①⑤⑦ (2)、①④⑧⑨⑾ ?②⑥⑿ ③⒁
(3)、②③⑥⑧⑩⑿⒀⒁ ③⒁ (4)、⑤ (5)④⑧⑨⑩⑾⒀
考查常见分子的空间构型及杂化轨道理论。
本题难度:一般
3、选择题 下列物质中,碱性最强的是
A.NaOH
B.Mg(OH)2
C.Al(OH)3
D.KOH
参考答案:D
本题解析:略
本题难度:一般
4、选择题 下列排列顺序正确的是(?)
① 热稳定性:H2O>HF>H2S?② 原子半径:Na>Mg>O
③ 酸性:H3PO4>H2SO4>HClO4?④ 熔沸点:H2O>HF>HCl
A.①③
B.②④
C.①④
D.②③
参考答案:B
本题解析:非金属性越强,氢化物的稳定性越强,①不正确,热稳定性应该是HF>H2O>H2S;同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则选项②正确;非金属性越强,最高价氧化物的水化物的酸性越强,③不正确,酸性应该是HClO4>H2SO4>H3PO4;水、HF分子间均存在氢键,熔沸点偏高,选项④正确,答案选B。
点评:该题主要是考查学生对元素周期律的熟悉了解程度,以及灵活运用元素周期律解决实际问题的能力,难度不大。该题的关键是熟练记住元素周期律的具体内容,然后结合题意灵活运用即可,有利于培养学生的逻辑思维能力和灵活应变能力。
本题难度:简单
5、选择题 下列关于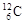 、
、 、
、 的说法正确的是 (?)
的说法正确的是 (?)
A.它们的化学性质不同
B.它们是碳元素的三种同位素
C.它们是碳元素的三种单质
D.它们是碳元素三种核素
参考答案:BD
本题解析:三种微粒核素具有相同的质子数,而具有不同的中子数,所以互为同位素,化学性质是相似,BD正确,AC错误,答案选BD。
点评:该题是高考中的常见考点,属于基础性试题的考查。侧重对学生灵活运用基础知识解决实际问题的能力的培养,有利于培养学生的逻辑思维能力和发散思维能力。
本题难度:简单