1、选择题 元素X的原子核外M电子层上有3个电子,元素Y2-的离子核外有18个电子,则这两种元素可形成的化合物为(?)
A.XY2
B.X2Y3
C.X3Y2
D.XY2
2、填空题  中的质子数是____________,中子数是____________,核外电子数是____________,质量数是____________。
中的质子数是____________,中子数是____________,核外电子数是____________,质量数是____________。
3、选择题 已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为:HXO4>H2YO4>H3ZO4,则下列判断中正确的是(? )?
A.元素非金属性按X、Y、Z的顺序减弱
B.原子的电子能力按X、Y、Z的顺序增强
C.气态氢化物的稳定性按X、Y、Z的顺序增强
D.单质的氧化性按X、Y、Z的顺序增强
4、选择题 元素R的最高价含氧酸的化学式为HnRO2n-2?,则在气态氢化物中R元素的化合价为(?)
A.12-3n
B.3n-12
C.3n-10
D.6-3n
5、填空题 元素周期表的形式多种多样,下图是扇形元素周期表的一部分,对照中学化学常见长式元素周期表,回答下列问题:
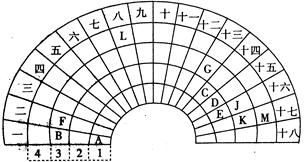
(1)元素C的最高价氧化物的电子式为?;元素G的离子结构示意图为?。
(2)元素L位于周期表的第?族, 1mol/L LM2溶液500ml与0.4 mol K单质恰好完全反应的离子方程式为_______________________________________。
(3)化合物X是由B、E、G三种元素组成,其水溶液呈_______性,原因是___________
_____________________________________________________(用离子方程式表示)
(4)D和G组成的化合物GD,被大量用于制造电子元件。工业上用G的氧化物、C单质和D单质在高温下制备GD,其中G的氧化物和C单质的则该反应的化学方程式为?。
(5)制取粗硅的过程中,SiO是反应中间产物,隔绝空气时SiO和NaOH溶液反应(产物之一是硅酸钠)的化学方程式______________________________________________