1、选择题 元素X的原子核外M电子层上有3个电子,元素Y2-的离子核外有18个电子,则这两种元素可形成的化合物为(?)
A.XY2
B.X2Y3
C.X3Y2
D.XY2
参考答案:B
本题解析:元素X的原子核外M电子层上有3个电子,则X是13号元素,是Al元素。元素Y2-的离子核外有18个电子,则Y是S元素。所以这两种元素可形成的化合物为Al2S3,答案选B。
点评:该题是中等难度的试题,主要是考查学生对元素化合价和最外层电子数关系的了解掌握情况,旨在培养学生灵活运用基础知识解决实际问题的能力,也有助于培养学生的逻辑推理能力,提高学生的应试能力。
本题难度:一般
2、填空题  中的质子数是____________,中子数是____________,核外电子数是____________,质量数是____________。
中的质子数是____________,中子数是____________,核外电子数是____________,质量数是____________。
参考答案:16? 18? 18? 34
本题解析:由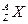 表示的含义知
表示的含义知 中Z=16、A=34,则N=34-16=18。因S2-是得到2个电子的二价阴离子,故核外电子数为16+2=18。
中Z=16、A=34,则N=34-16=18。因S2-是得到2个电子的二价阴离子,故核外电子数为16+2=18。
本题难度:简单
3、选择题 已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为:HXO4>H2YO4>H3ZO4,则下列判断中正确的是(? )?
A.元素非金属性按X、Y、Z的顺序减弱
B.原子的电子能力按X、Y、Z的顺序增强
C.气态氢化物的稳定性按X、Y、Z的顺序增强
D.单质的氧化性按X、Y、Z的顺序增强
参考答案:A
本题解析:据题意可知X为氯,Y为硫,Z为P 半径越小非金属性就越强。所以A选项是正确的
本题难度:一般
4、选择题 元素R的最高价含氧酸的化学式为HnRO2n-2?,则在气态氢化物中R元素的化合价为(?)
A.12-3n
B.3n-12
C.3n-10
D.6-3n
参考答案:B
本题解析:气态氢化物中元素一般为最低价态,根据化合物中化合价的代数和为0,R元素的最高价含氧酸中R的化合价为: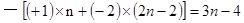 ,最低价的绝对值与最高价态的和为8,所以R的最低价态(为负值)为
,最低价的绝对值与最高价态的和为8,所以R的最低价态(为负值)为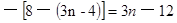 ,答案选B。
,答案选B。
本题难度:简单
5、填空题 元素周期表的形式多种多样,下图是扇形元素周期表的一部分,对照中学化学常见长式元素周期表,回答下列问题:
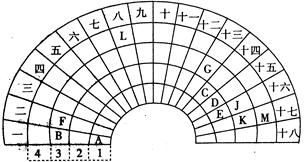
(1)元素C的最高价氧化物的电子式为?;元素G的离子结构示意图为?。
(2)元素L位于周期表的第?族, 1mol/L LM2溶液500ml与0.4 mol K单质恰好完全反应的离子方程式为_______________________________________。
(3)化合物X是由B、E、G三种元素组成,其水溶液呈_______性,原因是___________
_____________________________________________________(用离子方程式表示)
(4)D和G组成的化合物GD,被大量用于制造电子元件。工业上用G的氧化物、C单质和D单质在高温下制备GD,其中G的氧化物和C单质的则该反应的化学方程式为?。
(5)制取粗硅的过程中,SiO是反应中间产物,隔绝空气时SiO和NaOH溶液反应(产物之一是硅酸钠)的化学方程式______________________________________________
参考答案:(1)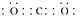 ?
?
(2)VIII? 10Fe2++6Br - +8Cl2=10Fe3++3Br2+16Cl-
(3)碱性,(1分) AlO2-+2H2O  Al(OH)3+OH-
Al(OH)3+OH-
(4)Al2O3+3C+N2  2AlN+3CO
2AlN+3CO
(5)? SiO+2NaOH=Na2SiO3+H2↑
本题解析:根据元素周期表中元素的相对位置,推A为氢、B为钠、C为碳、D为氮、E为氧、F为镁、G为铝、J为硫、K为氯、L为铁、M为溴。
(1)元素C的最高价氧化物为二氧化碳,电子式为 。元素G为铝,Al3+的离子结构示意图为
。元素G为铝,Al3+的离子结构示意图为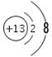 。
。
(1) ?
?
(2)元素L为铁,位于周期表的第VIII族? 1mol・L-1 LM2(FeBr2)溶液500mL与0.4 mol K单质(Cl2)的物质的量之比为5:4,恰好完全反应,因为还原性:Fe2+> Br-,因此Fe2+先被氧化:2Fe2++ Cl2 ?Fe3+ + 2Cl-,
?Fe3+ + 2Cl-,
每摩尔Fe2+反应用掉0.5molCl2,即按4:2反应,还剩余1.5mol的Cl2与Br-反应:2Br-+ Cl2 ?Br2 + 2Cl-,
?Br2 + 2Cl-,
注意只有3mol的Br-被Cl2氧化了,因为Cl2不足,整理得总反应:10Fe2+ +8Cl2+6Br- 10Fe3+ +16Cl- +3Br2。
10Fe3+ +16Cl- +3Br2。
(3)化合物X是NaAlO2,属于强碱弱酸盐, 水解显碱性,AlO2-+2H2O Al(OH)3+OH-。
Al(OH)3+OH-。
(4)化合物GD是AlN,G的氧化物是Al2O3,C单质是,D单质是氮气,Al2O3与C物质的量之比为1:3,用待定系数法。先假设Al2O3系数为1,C为3,可知AlN为2,N2为1,根据原子守恒,推知还生成3molCO,最后整理得Al2O3+3C+N2  2AlN+3CO。
2AlN+3CO。
(5)SiO和NaOH溶液反应,因为产物之一是酸钠,硅化合价由+2变为+4,化合价有升高,必然有化合价降低,分析可知,只有氢元素化合价可以降低,推出另一产物是氢气,配平得SiO+2NaOH=Na2SiO3+H2↑。
本题难度:一般