1������� þ�Ǻ�ˮ�к����϶�Ľ�����þ��þ�Ͻ���þ�Ļ������ڿ�ѧ�о���ҵ��������;�dz��㷺��
��1��Mg2Ni��һ�ִ���Ͻ���֪��
Mg(s) + H2(g)=MgH2(s) ��H1=��74.5kJ��mol��1
Mg2Ni(s) + 2H2(g)=Mg2NiH4(s) ��H2=��64.4kJ��mol��1
Mg2Ni(s)+2MgH2(s) = 2Mg(s)+Mg2NiH4(s)?��H3
���H3 =?kJ��mol��1��
��2����ҵ�Ͽ��õ�����ڵ���ˮ�Ȼ�þ���þ�������Ȼ�þ��ˮ�ǹؼ�����֮һ��һ������������Ȼ�þ������ˮ�ķ����ǣ��Ƚ�MgCl2��6H2Oת��ΪMgCl2��NH4Cl��nNH3���þ���Σ�,Ȼ����700���Ѱ��õ���ˮ�Ȼ�þ���Ѱ���Ӧ�Ļ�ѧ����ʽΪ?����������Ȼ�þ�������ĵ缫��ӦʽΪ?��
��3���������Mg(AlH4)2��110-200��C�ķ�ӦΪ��Mg(AlH4)2=MgH2 +2A1+3H2��ÿ����27gAlת�Ƶ��ӵ����ʵ���Ϊ?��
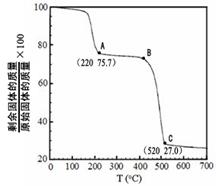
��4����ҵ����MgC2O4��2H2O�ȷֽ��Ƴ�ϸMgO�����ȷֽ�������ͼ��
ͼ�и�������������B��C������Ӧ�Ļ�ѧ����ʽΪ?��
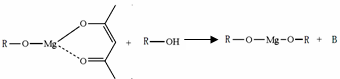
��5��һ���л�þ����������������ѧԪ����Ϳ��Һ����ѧʽ�ɱ�ʾΪ��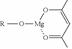 �����ɷ������·�Ӧ��
�����ɷ������·�Ӧ��
ROH��B�ĺ˴Ź�����������ͼ:
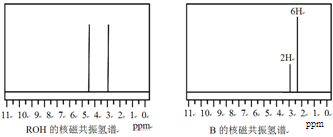
ROH��C��H��O��F����Ԫ����ɵĺ����л��������ֻ��1����ԭ�ӣ����з�ԭ�ӻ�ѧ������ͬ����Է�������Ϊ168����ROH�Ľṹ��ʽΪ?�� B�Ľṹ��ʽΪ?��
�ο��𰸣�
��1��+84.6��2�֣���
��2��MgCl2��NH4Cl��nNH3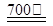 MgCl2 +(n+1)NH3�� + HCl��?��2�֣���? Mg2++2e��= Mg��2�֣���
MgCl2 +(n+1)NH3�� + HCl��?��2�֣���? Mg2++2e��= Mg��2�֣���
��3��3mol��2�֣�����4��MgC2O4 MgO + CO��+ CO2����2�֣�
MgO + CO��+ CO2����2�֣�
��5��(CF3)2CHOH ��2�֣���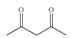 ��2�֣���
��2�֣���
�����������1������ʽ�ڣ��١�2=��64.4������74.5����2=+84.6 kJ��mol��1����2��������ֽ�õ���ˮ�Ȼ�þ�����������Ȼ��⣻���������ӷŵ磻��3���÷�Ӧ��ֻ����Ԫ�ػ��ϼ۽��ͣ���+3�۵�0�ۣ�����1mol��������ת��3mol����4������ͼ���ݼ����������������Ϊ148g����һ�ηֽ��������Ϊ148��75.7%=112g���ڶ��ηֽ���������Ϊ148��27%=40g������A������MgC2O4��C������MgO��B��C������ӦΪMgC2O4 MgO + CO��+ CO2������5��������Ϣ����1���ǻ���ͼ������ʾ�����к���2�л�ѧ������������Ŀ��ͬ����������ֻ����������ԭ�ӣ�����ȫ����ȡ����������Է�������ȷ��Ϊ(CF3)2CHOH��
MgO + CO��+ CO2������5��������Ϣ����1���ǻ���ͼ������ʾ�����к���2�л�ѧ������������Ŀ��ͬ����������ֻ����������ԭ�ӣ�����ȫ����ȡ����������Է�������ȷ��Ϊ(CF3)2CHOH��
�����Ѷȣ�һ��
2�������� ��֪����ѧ��Ӧ3Ag+ 4HNO3 ��ϡ��= 3AgNO3+ NO��+ 2H2O?
��1���÷�Ӧ�����ӷ���ʽΪ��_________________________________? ____
��2������32.4�����ܽ�ʱ����Ӧ���ɵ�NO�ڱ���µ�����Ƕ��٣�
��3������0.2mol���ܽ�ʱ���ж��ٿ�HNO3����ԭ��
�ο��𰸣���1��3Ag+4H++NO3-=3Ag++NO��+2H2O
��2��2.24L?��3��4.2g
���������������ݷ���ʽ���е��йؼ��㡣
��1�����ݻ�ѧ����ʽ��֪���÷�Ӧ�����ӷ���ʽΪ3Ag+4H++NO3-=3Ag++NO��+2H2O��
��2��32.4g����324g��108g.mol��0.3mol�����Ը��ݷ���ʽ��֪����NO��0.1mol����״���µ������2.24L��
��3��0.2mol��ʧȥ0.2mol���ӡ�ϡ���ڷ�Ӧ�еõ�3�����ӣ����Ա���ԭ�������� ��
��
�����Ѷȣ�һ��
3��ѡ���� ij�¶��½�Cl2ͨ��KOH��Һ���Ӧ��õ�KCl��KClO��KClO3�Ļ����Һ����Cl2��KOH��Һ��Ӧʱ������ԭ�뱻��������Ԫ�����ʵ���֮����11�U3������Һ��ClO-��ClO3-�����ʵ���֮���ǣ�?��
A��1�U1
B��1�U2
C��1�U3
D��2�U1
�ο��𰸣�B
�������������Һ��ClO-��ClO3-�����ʵ����ֱ���x��y����ԭ����ԭ����11(x��y)/3�����Ը��ݵ��ӵĵ�ʧ�غ��֪��11(x��y)/3��x��5y�����x�Uy��1�U2��ѡ��B��ȷ����ѡB��
�����Ѷȣ�һ��
4��ѡ���� �������巨����Cr2O72-�ķ�ˮ��ԭ���ɸ���Ϊ����Cr2O72-�����Է�ˮ�м��� FeSO4��7H2O ����Cr2O72-��ԭΪCr3+��������Һ�� pH��ʹ��Һ�е�������Ԫ��ת��Ϊ����൱��Fe��[Fe�� XCr�� 2-X]O4���������塢 �������ֱ�ʾԪ�صļ�̬���ij����������� 1 mol Cr2O72-�ķ�ˮ������Ҫ����amol FeSO4��7H2O?�����н�����ȷ����
�������ֱ�ʾԪ�صļ�̬���ij����������� 1 mol Cr2O72-�ķ�ˮ������Ҫ����amol FeSO4��7H2O?�����н�����ȷ����
A��x= 0��5 , a=" 8"
B��x = 0��5 , a="10"
C��x = 1��5 , a=" 8"
D��x = 1��5 , a= 10
�ο��𰸣�D
�����������
�����Ѷȣ���
5������� �����12�֣�Ԫ�����ڱ��Т�A��Ԫ�صĵ��ʼ��仯�������;�㷺��
23������Ԫ��ͬ��Ķ�����Ԫ�ص�ԭ�ӣ������������ߵĵ��������ĵ����Dz��� ��
24����Ԫ����Ԫ�����ڱ��е�λ���� ��Ϊ��ȱ�⣬ʳ���г����ӵ���أ��������ڴ��� �����ѧ�����ͣ���
25���嵥����Ψһ�����³�Һ̬�ķǽ������ʣ����ĵ���ʽ�� ��Һ��ı���ͨ����ȡ�ķ����� ��
26��ͨ���Ƚ�___________��________________�����ж��ȡ�������Ԫ�طǽ�����ǿ����
27����ҵ�ϣ�ͨ������ת�����Ƶ�KClO3���壺
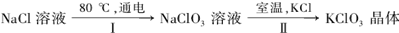
����ƽI�з�Ӧ���ܻ�ѧ����ʽ�����������ת�Ƶķ������Ŀ��
��NaCl + ��H2O 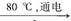 ��NaClO3+ ��
��NaClO3+ ��
��II��Ӧ����������KClO3���������������������ԭ���� ��
28��CuCl(s)��O2��Ӧ����CuCl2(s)��һ�ֺ�ɫ���塣��25�桢101kPa�£���֪�÷�Ӧ����1 mol CuCl(s)������44.4 kJ���÷�Ӧ���Ȼ�ѧ����ʽ��_________________________��
�ο��𰸣�23��2p ��1�֣� 24���������ڢ�A�壨1�֣� ���Ӽ������ۼ���1�֣�
25��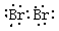 ��1�֣� ˮ������ɫƿ�У��ܱձ��棨1�֣�
��1�֣� ˮ������ɫƿ�У��ܱձ��棨1�֣�
26��HCl��HBr����̬�⻯������ȶ��ԡ�HClO4��HBrO4������ ��2�֣����������ɣ�
27����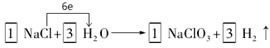 ��H2 ��ϵ��1�֣�������Ŀ1�֣�
��H2 ��ϵ��1�֣�������Ŀ1�֣�
�������£��������ˮ�е��ܽ������С���������壨1�֣�
28��4CuCl(s) + O2(g)=2CuCl2(s) + 2CuO(s)��H=��177.6kJ/mol ��2�֣�
���������23������Ԫ��ͬ��Ķ�����Ԫ��FԪ�ص�ԭ�Ӻ�����9�����ӣ����������Ų�ʽ��1s22s22p5���ɼ���������ߵĵ��������ĵ����Dz���2p�Dz㣻
24��53��Ԫ�ص�Ԫ�غ�����5�����Ӳ㣬�������7�����ӣ�������Ԫ�����ڱ��е�λ���ǵ������ڢ�A�壻Ϊ��ȱ�⣬ʳ���г����ӵ���أ������������ӻ�����ڴ������Ӽ������Թ��ۼ���
25���嵥����Ψһ�����³�Һ̬�ķǽ������ʣ�����˫ԭ�ӷ��ӣ�����ԭ�ӹ���һ�Ե��ӣ����ﵽ8�����ӵ��ȶ��ṹ�����ĵ���ʽ��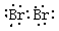 ��Һ�����ӷ����������ܶȱ�ˮ����ˮ���ܽ�Ȳ�������Һ��ͨ�������ȡ����ɫƿ�ڣ�����ˮ�γ�ˮ�⣬�ܷⱣ�档
��Һ�����ӷ����������ܶȱ�ˮ����ˮ���ܽ�Ȳ�������Һ��ͨ�������ȡ����ɫƿ�ڣ�����ˮ�γ�ˮ�⣬�ܷⱣ�档
26��Ԫ�صķǽ�����Խǿ������Ӧ���⻯����ȶ��Ծ�Խǿ����۵ĺ����������ҲԽǿ�����Կ���ͨ���Ƚ�HCl��HBr����̬�⻯������ȶ��ԡ�HClO4��HBrO4�����Կ����ж��ȡ�������Ԫ�طǽ�����ǿ����
27���������ڷ�Ӧ��ClԪ�صĻ��ϼ����ߣ������������ԭ��Ӧ�Ĺ��ɣ���Ӧ����Ԫ�صĻ��ϼ۽��ͣ�ֻ��HԪ�ط��Ÿ����ʣ��õ����ӱ�ΪH2����ϵ����غ㼰ԭ���غ�ɵ÷���ʽΪ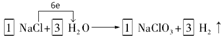
��II��Ӧ����������KClO3�����������������������Ϊ�����£��������ˮ�е��ܽ������С����������
28��CuCl(s)��O2��Ӧ����CuCl2(s)��һ�ֺ�ɫ���塣��25�桢101kPa�£���֪�÷�Ӧ����1 mol CuCl(s)������44.4 kJ����������ɵø÷�Ӧ���Ȼ�ѧ����ʽ��4CuCl(s) + O2(g) = 2CuCl2(s) + 2CuO(s) ��H=��177.6kJ/mol��
���㣺����ԭ�Ӻ�����ӵ��Ų��������ڵĻ�ѧ�������͵��жϡ����ʵ���ʽ����д�����ʵı��桢Ԫ�طǽ�����ǿ���Ƚϡ�������ԭ��Ӧ����ʽ����ƽ���Ȼ�ѧ����ʽ����д��֪ʶ��
�����Ѷȣ�����