1��ѡ���� Mg-AgCl�����һ���ú�ˮ�����һ�ε�أ��ھ����������綯���ĵ�Դ����ص��ܷ�Ӧ�ɱ�ʾΪ��Mg+2AgCl=MgCl2+2Ag�����й��ڸõ��˵���������
A���õ�ع���ʱ��������ӦΪ��2AgCl+2e-=2Cl-+2Ag
B��þ�缫���õ�ظ�����������ӦΪ��Mg-2e-=Mg2+
C������24g Mg������ʱ����108 g Ag����ԭ
D��װ���õ�ص�������ˮ���н�ʱ����ˮ��Ϊ�������Һ
�ο��𰸣�C
����������ܷ�ӦʽΪ��Mg+2AgCl=MgCl2+2Ag
������ӦΪ��2AgCl+2e-=2Cl-+2Ag��������ӦΪ��Mg-2e-=Mg2+
�ɷ���ʽ�ɼ������24 g Mg������ʱ����216 g Ag����ԭ
�����Ѷȣ�һ��
2������� ��ʵ�������
����A��B��C��D��E���ֳ���������Ԫ�أ���֪��
��Ԫ�ص�ԭ��������A��B��C��D��E��������ԭ�Ӱ뾶��D��E��B��C��A˳�����μ�С��
��A��Dͬ���壬A������Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ�B��C��λ�����ڣ�CԪ��ԭ�������������Ǵ�����������3����
��B��D��E���ߵ������������ˮ��������Ϊ�ס��ҡ�������������֮����ɷ�Ӧ���ɿ������κ�ˮ�����������о���CԪ�أ�
��B��E����Ԫ��ԭ������������֮�͵���A��C��D����Ԫ��ԭ������������֮�͡�
����д���пհף�
��1��д����+������Һ�з�Ӧ�����ӷ���ʽ______________________________________________________________________��
��2�� ������BA3��BC�ڼ��Ⱥ��д������ڵ��������ܷ�����Ӧ���������������ʣ��䷴Ӧ�Ļ�ѧ����ʽΪ��___________________________________________��
��3�� ijԭ����У��������ҺΪϡH2SO4,�ֱ���ͨ��̼Ԫ����Ԫ��C��ԭ�����ʵ���֮��1��1���γɵĻ�����,������ͨ��Ԫ��C����ĵ���,������������⣺
������Ӧ��________________________��
������Ӧ��________________________��
�������ҺpH�ı仯_______��(�������С�����䡱����ͬ)
�ο��𰸣�17����1��Al(OH)3��OH-=[Al(OH)4]- ��2��4NH3 + 6NO = 5N2 +6 H2O
��3��������Ӧ��O2+4e-+4H+=4H2O,������Ӧ��2CO-4e-+2H2O=2CO2+4H+, ����
���������A��B��C��D��E���ֳ���������Ԫ�أ�Ԫ�ص�ԭ��������A��B��C��D��E��������A��Dͬ���壬A������Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ���AΪ��Ԫ�أ�DΪ��Ԫ�أ�CԪ��ԭ�������������Ǵ�����������3����Cֻ������Ԫ�أ�B��C��λ�����ڣ�B���ǵ�Ԫ�أ�B��D��E���ߵ������������ˮ��������Ϊ�ס��ҡ�������������֮����ɷ�Ӧ���ɿ������κ�ˮ�����������о���CԪ�أ���EΪ��Ԫ�ء���1����Ϊ�������ƣ���Ϊ��������������+������Һ�з�Ӧ�����ӷ���ʽ��Al(OH)3��OH-=[Al(OH)4]-����2��������BA3��NH3����BC(NO)�ڼ��Ⱥ��д������ڵ��������ܷ�����Ӧ����������������Ϊ������ˮ���䷴Ӧ�Ļ�ѧ����ʽΪ��4NH3 + 6NO = 5N2 +6 H2O;��3�� ̼Ԫ����Ԫ��C��Ϊ��Ԫ�أ���ԭ�����ʵ���֮��1��1���γɵĻ�����ΪCO����������дCOȼ�ϵ�صĵ缫��Ӧ������������Ӧ��O2+4e-+4H+=4H2O,������Ӧ��2CO-4e-+2H2O=2CO2+4H+,CO������������ȼ������CO2����˵������ҺpH���䡣
���㣺����ԭ�ӽṹ�Ļ���֪ʶ����ѧ����ʽ��ȼ�ϵ�ص�֪ʶ��
�����Ѷȣ�һ��
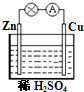
3��ѡ���� ����п��ͭ��ϡ������ɵ�ԭ��أ���ͼ���������й�˵����ȷ���ǣ�������
��Zn�Ǹ���?�ڵ�����Zn�����·����Cu
��Zn-2e-�TZn2+?��Cu2+����Һ����Cu����Zn��Ǩ�ƣ�
A���٢�
B���٢ڢ�
C���ڢۢ�
D���٢ڢۢ�