1��ѡ���� ʵ��������һƿ���õİ�ɫ��ĩ��Ԫ�ط���֤�������ɼء���������Ԫ����ɣ��غ����������Ϊ39��16�����н�����ȷ���ǣ�������
A������Ԫ�ط�������Ʋ�÷�ĩΪ������
B������ĩ����ˮ�������Ȼ������۲쵽�а�ɫ�������ɣ�֤��ԭ��ĩ�������
C������ĩ���������У��������ݣ�֤��ԭ��ĩ���������
D������ĩ����ˮ�������Ȼ��������ᣬ�۲쵽�а�ɫ�������������ɣ�֤��ԭ��ĩ������غ�������صĻ����
�ο��𰸣�D
���������
�����Ѷȣ���
2��ѡ���� ��ʵ���ң���ȡһ�����Ĵ��ξ��ܽ⡢���ˡ��ᾧ�Ȳ������ɵõ��ϴ�����ʳ�Σ�����ͼʾ��Ӧ�IJ������淶���ǣ� ? ��
A��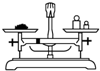
����
B��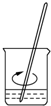
�ܽ�
C��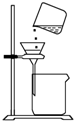
����
D��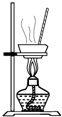
�ᾧ
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3������� Ϊ�ⶨ��������茶��塾��NH4��2Fe��SO4��2?xH2O�������ĺ�����ijʵ��С����������ʵ�飺
����һ���õ�����ƽȷ����5.000g��������茶��壬���Ƴ�250ml��Һ��
�������ȡ������Һ25.00ml����ƿ�У���ϡH2SO4�ữ����0.010mol/LKMnO4��Һ�ζ���Fe2+ǡ��ȫ��������Fe3+��ͬʱ��MnO4-����ԭ��Mn2+��
���ظ���������Σ�
��ش��������⣺
��1�����������������Һ�IJ������������ǣ�������______��ת�ơ�ϴ�Ӳ�ת�ơ�______��ҡ�ȣ�
��2����______�ζ���ʢ��KMnO4��Һ��
��3�����������һ��KMnO4��Һ������______��������ζ��յ㣮��Ӧ�����ӷ���ʽ��______
��4���ζ�������±���ʾ��
| �ζ����� | ������Һ�����/mL | ����Һ�����
�ζ�ǰ�̶�/mL
�ζ���̶�/mL
1
25.00
1.05
21.04
2
25.00
1.50
24.50
3
25.00
0.20
20.21
|
ʵ���øþ�����������������Ϊ______����������λС����
��5�����ݲ������գ�
�ٵζ���������ˮϴ�Ӻ�ֱ�Ӽ���KMnO4����Һ���еζ���������Ʒ����������������______�����ƫ�ߡ�����ƫ�͡�����Ӱ�족����
����ƿ������ˮϴ�Ӻ�δ�����ζ�ʱ��ȥKMnO4����Һ�������______���ƫ����ƫС������Ӱ�족����
�۵ζ�ʱ�ߵα�ҡ����ƿ���۾�Ӧ�۲�______��
A���ζ�����Һ��ı仯B����ƿ����Һ��ɫ�ı仯
�ܵζ����Ӷ����������Ʒ����������������______���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
�ο��𰸣���1��������Һ��Ҫ�������ܽ⡢ת�ơ�ϴ�Ӳ�ת�ơ����ݡ�ҡ�ȵȲ������ʴ�Ϊ���ܽ⣻���ݣ�
��2��KMnO4��Һ����ǿ�����ԣ�Ӧ����ʽ�ζ���ʢװ�ʴ�Ϊ����ʽ��
��3��Fe2+��KMnO4����������ԭ��Ӧ����Ӧ�����ӷ���ʽΪMnO4-+5Fe2++8H+�TMn2++5Fe3++4H2O��
�ζ��յ�ʱ����Һ�ɻ�ɫ����Ϻ�ɫ���Ұ�����ڲ���ɫ��
�ʴ�Ϊ����Һ�ɻ�ɫ����Ϻ�ɫ���Ұ�����ڲ���ɫ��MnO4-+5Fe2++8H+�TMn2++5Fe3++4H2O��
��4��ȡ������Һ25.00ml����ƿ�У���ϡH2SO4�ữ����0.010mol/LKMnO4��Һ�ζ������ø��������Һ���Ϊ21.04-1.05+24.50-1.50+20.21-0.203mL=21mL��
n��MnO4-��=0.021L��0.01mol/L=2.1��10-4mol��
��n��Fe2+��=5��2.1��10-4mol=1.05��10-3mol��
5.000g��������茶��庬��n��Fe2+��=1.05��10-2mol��
n��Fe2+��=56g/mol��1.05��10-2mol=0.588g��
ʵ���øþ�����������������Ϊ0.588g5.00g��100%��11.20%��
�ʴ�Ϊ��11.20%��
��5�����ٵζ���������ˮϴ�Ӻ�ֱ�Ӽ���KMnO4����Һ���еζ����ζ���û����ϴ��Ũ��ƫ�ͣ����ƫ�ⶨ�ṹƫ�ߣ��ʴ�Ϊ��ƫ�ߣ�
����ƿ�Ƿ����Եζ����û��Ӱ�죬�ʴ�Ϊ����Ӱ�죻
�۵ζ�ʱ�ߵα�ҡ����ƿ���۾�Ӧ�۲���ƿ����Һ��ɫ�ı仯���ʴ�Ϊ��B��
�ܵζ����Ӷ������ᵼ�����ƫС���ʴ�Ϊ��ƫ�ͣ�
���������
�����Ѷȣ���
4������� ʳ��ˮ�к��п����Ե�CaCl2��MgCl2��Na2SO4�����ʣ�ͨ�����¼���ʵ�鲽�裬���Ƶýϴ�����ʳ��ˮ��
�ټ����Թ�����Na2CO3��Һ
�ڼ����Թ�����NaOH��Һ
�ۼ����Թ�����BaCl2��Һ
�ܵ���ϡ�����������ݲ���
�ݹ���
��ȷ�IJ���˳����______��
�ο��𰸣�����Ҫ�Ѵ�������ˮ�γ���Һ��Ȼ��þ���������������ӳ���������������������ƿ��Խ�þ���ӳ���������������ñ����ӳ���������������Ȼ������Խ���������ӳ����������ȳ�þ���ӣ������ȳ���������Ӷ��У���������̼������ӳ������������Ӽ���̼����ת��Ϊ���������Ǽ����̼����Ҫ���ڼ�����Ȼ���֮������̼���ƻ��ȥ��Ӧʣ����Ȼ��������Ӷ������ˣ��ٽ��й��ˣ�����ټ��������ȥ��Ӧʣ������������Ӻ�̼������ӣ�������������õ��ϴ������Ȼ��ƣ�������ȷ��˳��Ϊ�ۢڢ٢ݢܣ�
��ѡA��
���������
�����Ѷȣ�һ��
5��ѡ���� ����ʵ������д�����ǣ�������
A�����������б����ò��������Ͻ��裬�Է�ֹ�ֲ��¶ȹ��߶�ʹҺ��ɽ�
B���������ʱ��Ӧʹ�¶ȼ�ˮ����������ƿ��֧�ܿڴ�
C����Һ����ʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ���
D����ȡ����ʱ��Ӧѡ���л���ȡ��������ȡ�����ܶȱ����ˮ��
�ο��𰸣�D
���������
�����Ѷȣ���