1��ѡ���� Ԫ�ء�����﨡�嵐��������������ֿ�ѧ�������ֵģ�
A���������
B������
C��ԭ�ӹ���
D���˴Ź�����
2��ѡ���� 1862��һλӢ����ѧ�Ҹ���O2��Xe�ĵ�һ�����ܷdz��ӽ����������˼��ϳɵ�һ��ϡ�����廯�������ƶ��˶�ϡ��������о���Ϊ����ϡ�����廯ѧ��������ʷ�ԵĹ��ס��û�ѧ��Ϊ��?��
A���Ͷ�ĩ
B��������
C������
D�����»�
3������� ��15�֣����Ų��Ͽ�ѧ�ķ�չ�����������仯����õ���Խ��Խ�㷺��Ӧ�ã�������Ϊ���Ͻ��ά���ء���Ϊ�������ú�������������V2O5��VOSO4�������Բ�������������Ա����������һ�����ӽ��������շ����¹��գ������ʴ�91.7%���ϡ�
���ֺ���������ˮ�е��ܽ������±���ʾ��
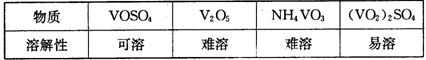
�ù��յ���Ҫ�������£�
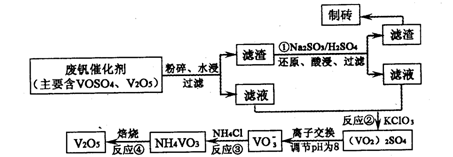
��ش��������⡣
�Ź�ҵ����V2O5ұ���������������ȼ������û�ѧ����ʽ��ʾΪ?��
�Ʒ�Ӧ�ٵ�Ŀ����?��
�Ǹù����з�Ӧ�۵ij����ʣ��ֳƳ����ʣ��ǻ��շ��Ĺؼ�֮һ��д���ò�������Ӧ�����ӷ���ʽ��?��
������֪Ũ�ȵ������ữ��H2C2O4��Һ���ζ���VO2��2SO4��Һ���Բⶨ��Ӧ�ں���Һ�к�������VO2++H2C2O4+H+��VO2++CO2+X��
XΪ?��д��ѧʽ����

�ɾ������ط�����ã�NH4VO3�ڱ��չ����У����������ļ���ֵ�������꣩���¶ȱ仯����������ͼ��ʾ����NH4VO3�ڷֽ������?������ţ���
A���ȷֽ�ʧȥH2O���ٷֽ�ʧȥNH3
B���ȷֽ�ʧȥNH3���ٷֽ�ʧȥH2O
C��ͬʱ�ֽ�ʧȥH2O��NH3
D��ͬʱ�ֽ�ʧȥH2��N2��H2O
4��ѡ���� ����������ȷ���ǣ�?��
A����ˮ���̺���Ԫ����80���֣�����Mg��Br��I�ں�ˮ�е��ܴ����ֱ�ԼΪ1.8��1015t��1��1014t��8��1010t�����ں�ˮ��þ�Ĵ����ܴ�ҵ�ϳ��Ժ�ˮΪԭ����ȡþ����ˣ�þԪ�ر���Ϊ������Ԫ�ء�
B�����ڿ��淴ӦN2��g��+3H2��g��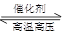 2NH3��g����������Ũ�ȿ����ӻ���Ӱٷ������Ӷ�ʹ��Ӧ��������
2NH3��g����������Ũ�ȿ����ӻ���Ӱٷ������Ӷ�ʹ��Ӧ��������
C�����Ṥҵ�У����������ϲ������������ٴ�ͨ��Ӵ��ҽ��ж�����������һ�����պ�������ĺ������٣���ֱ���ŷŵ�������
D���������ߺͦ�-����ɢ������ԭ�ӽṹģ�͵Ľ��������˹���
5������� (14��) ��ӡ��ʹ�õ�ī����Ҫ�ɷ���Fe3O4����ͼ����������������Fe3O4�Ĺ��գ�
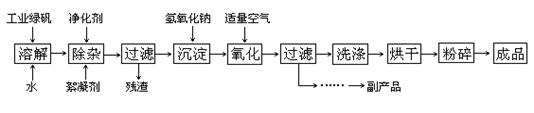
��֪���ٹ�ҵ�̷���FeSO4�ĺ���Ϊ52.5%�����е����ʲ����뷴Ӧ��
��? Fe(OH)2��2Fe(OH)3��Fe3O4��4H2O?
��? 12.16�~1000�~52.5%=6384,6384��152=42��ش��������⣺
��1�����ij�����������?��
��2��Fe3O4��ϡ���ᷴӦ�����ӷ���ʽ��?�����鷴Ӧ�����Һ�к�Fe3+�ķ���?��
��3���ڹ��������У�ͨ������������������ʱ�Ļ�ѧ����ʽ�ǣ�?��
��4�������пɻ�õĸ���Ʒ��?����ȡ�ø���Ʒ�IJ���˳����?����д��ţ�
a������? b������Ũ��? c����ȴ? d���ᾧ? e��ϴ��
��5�������������У�����ҵ�̷���Ͷ��������12.16 kg/h��Ϊʹ��Ʒ�ϴ����������������ӦΪ?L/h�����跴Ӧ�ڱ�״̬�½��У�������O2ռ20%����