1、填空题 依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_______________________________。
(2)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量
____________________________。
(3)已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_____________________________。
2、选择题 下列热化学方程式或说法正确的是
[? ]
A.甲烷的燃烧热为△H=-890 kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+
2H2O(g) △H=-890 kJ/mol
B.500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)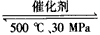 2NH3(g) △H=-38.6 kJ/mol
2NH3(g) △H=-38.6 kJ/mol
C.已知:H2(g)+F2(g)=2HF(g) △H= -270 kJ/mol,则1mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ
D.在C中相同条件下,2 mol HF气体的能量小于1 mol 氢气与1mol氟气的能量总和
3、填空题 (1)已知:2SO2(g)+O2(g)?2SO3?(g)△H=-196.6kJ?mol-1;2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1 .则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=______kJ?mol-1
一定条件下,将NO2与SO2?按体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是______.
a.体系压强保持不
b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变
d.每消耗1mol SO3的同时生成1mol NO2
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图1所示.该反应△H______0(填“>”或“<”).实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是______
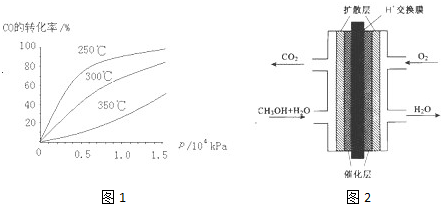
(3)甲醇(CH3OH)燃料电池的结构示意图如图2.甲醇进入______极(填“正”或“负”),正极发生的电极反应为______.
(4)101kPa时,若16gCH3OH完全燃烧生成液态水,放出热量为363.25kJ/mol,则甲醇燃烧的热化学方程式为______.
4、选择题 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0 kJ・mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ・mol-1
下列说法正确的是
[? ]
A.CH3OH的反应热不仅与各物质的状态有关,也与参加反应的反应物的量有关
B.CH3OH蒸气的燃烧热大于676.7kJ・mol-1
C.CH3OH转变成H2的过程只能是一个从高能量到低能量的过程
D.根据①推知反应:CO2(g)+3H2(g)=CH3OH(l)+H2O(g) 的△H<-49.0kJ・mol-1
5、选择题 国际石油价格多次上涨,为解决能源危机,多省市推广使用乙醇汽油作为发动机燃料,即在汽油中掺入一定比例的乙醇,以代替一部分汽油。已知热化学方程式:1/2C2H5OH(l)+ 3/2O2(g)=CO2(g)+3/2H2O(l)△H=-683.4kJ/mol。下列有关说法正确的是
[? ]
A.乙醇汽油是一种清洁能源,燃烧不会产生任何污染
B.在25℃、101kPa时,生成1mol水时放出683.4kJ的热量
C.乙醇的燃烧热为1366.8kJ/mol
D.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) △H=-1366.8kJ/mol