1、实验题 铁在冷的浓硫酸中能发生钝化。某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。实验室现有下列试剂:0.01 mol/L酸性KMnO4溶液、0.1 mol/L KI溶液、3%H2O2溶液、淀粉溶液、蒸馏水。请你协助他们探究所得溶液和气体的成分。
(1)【提出猜想】
Ⅰ.所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种;
Ⅱ.所得气体中可能含有________中的一种或两种。
(2)【实验探究】


(3)【问题讨论】有同学提出,若另外选用KSCN溶液,则仅利用KSCN和H2O2两种溶液即可完成猜想Ⅰ的所有探究,请对该观点进行评价:_______________________________。
参考答案:(1)SO2、H2?
(2)猜想Ⅰ:步骤①酸性KMnO4溶液紫红色褪去;含有Fe2+
步骤②另取少量所得溶液,滴加KI和淀粉溶液;溶液变为蓝色
猜想Ⅱ:甲中KMnO4溶液褪色,乙中KMnO4溶液颜色不变,试管中收集到气体
(3)不正确,若溶液中含有Fe3+则无法检验溶液中是否含有Fe2+
本题解析:
本题难度:一般
2、选择题 为使人们确知含碘物质的存在,研究性学习小组同学设计了一种简便的检验方法,利用该物质在酸性条件下与KI反应有单质碘生成的性质,选用下列生活常见的物质就可完成.请你从下列物质中选出合适的一组?( )
①自来水 ②食醋 ③淀粉 ④食糖 ⑤碘化钾试纸 ⑥碘酒?
A.①③④⑤
B.②③④⑤?
C.①③⑤⑥
D.②③⑤
参考答案:食醋能提供酸性环境,碘化钾溶液能提供碘离子,碘与淀粉变蓝色,所以淀粉能提供反应物,故选D.
本题解析:
本题难度:简单
3、实验题 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。 请回答该实验中的问题。

(1)写出该反应的化学方程式__________________,其中氧化剂是________,还原剂是_________。
8.4g铁粉参加反应,转移电子_________mol。
(2)玻璃管中石棉绒的作用是_______________,实验开始时应先点燃___________,实验结束时应先熄灭______________。
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是__________________________;烧瓶底部应事先放置_________________,其作用是________________________。
参考答案:(1)3Fe+4H2O(g) Fe3O4+4H2;H2O;Fe;0.4
Fe3O4+4H2;H2O;Fe;0.4
(2)铁粉的载体,增大铁粉与水蒸气的接触面;酒精灯;酒精喷灯
(3)为实验提供水蒸气;碎瓷片;防止暴沸
本题解析:
本题难度:一般
4、选择题 用下图所示装置进行实验,不能达到实验目的的是:(?)
 ?
? ?
?
甲?乙
 ?
?
丙?丁
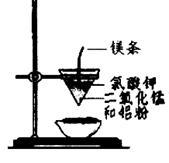
A.用甲装置比较硫、碳、硅三种元素的非金属性强弱
B.用乙装置可制得金属锰,用同样的装置可制得金属铬
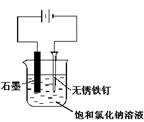
C.用丙装置可实现对铁钉的保护
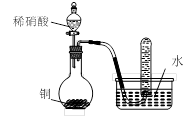
D.用丁装置验证铜与稀硝酸反应的气体产物只有NO
参考答案:D
本题解析:A、要比较硫、碳、硅三种元素的非金属性强弱,则可以通过最高价氧化物对应水化物的酸性强弱比较,依据较强的酸制备较弱的酸可知,用甲装置比较硫、碳、硅三种元素的非金属性强弱,A正确;B、锰可以通过铝热反应制备,B正确;C、铁钉与电源的负极相连,作阴极,属于外加电流的阴极保护法,C正确;D、由于NO2溶于水即可生成NO,所以不能用丁装置验证铜与稀硝酸反应的气体产物只有NO,D不正确,答案选D。
本题难度:一般
5、实验题 某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
[实验]制备银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
(1)下列有关制备银镜过程的说法正确的是____________________。
a.边振荡盛有2%的AgNO3溶液的试管,边滴入2%的氨水。至最初的沉淀恰好溶解为止
b.将几滴银氨溶液滴入2 mL乙醛中
c.制备银镜时,用酒精灯的外焰给试管底部加热
d.银氨溶液具有较弱的氧化性
e.在银氨溶液配制过程中,溶液的pH增大
[提出假设]
假设1:Fe3+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3溶液显酸性,在此酸性条件下NO3-能氧化Ag。
[设计实验方案,验证假设]
(2)甲同学从上述实验的生成物中检验出Fe3+,验证了假设1成立。请写出Fe3+氧化Ag的离子方程式:
________________________。
(3)乙同学设计实验验证假设2,请帮他完成下表中内容(提示:NO3-在不同条件下的还原产物较复杂,有时难以观察到气体产生)。

[思考与交流]
(4)甲同学验证了假设1成立,若乙同学验证了假设2也成立。则丙同学由此得出结论:Fe(NO3)3溶液中的Fe3+和NO3-都氧化了Ag。你是否同意丙同学的结论,并简述理由:_________________________。
参考答案:(1)ade
(2)Fe3++Ag==Fe2++Ag+
(3)将银镜在硝酸铜溶液中
(4)同意,4Fe3++6H2O+9Ag+3NO3-==4Fe(OH)3↓+9Ag++3NO↑
本题解析:
本题难度:困难