1、简答题 25℃时,几种弱酸溶液的pH如下表所示:
| 弱酸 | CH3COOH | H2SO3 | HCN
物质的量浓度mol/L
0.01
0.01
0.01
pH
3.4
2.3
5.6
|

(1)25℃时,Na2SO3溶液的pH______(填“>”、“<”“或“=”)7,其原因是______(用离子方程式表示).
(2)图1是常温下,相同pH的CH3COOH和HCN溶液分别加水稀释时溶液的pH随溶液体积变化的曲线.
①图1中曲线______(填“Ⅰ”或“Ⅱ”)表示加水稀释HCN溶液时pH的变化.
②下列操作能使CH3COOH的电离程度与同时增大的是______.
A.加水稀释溶液? B.升高溶液温度? C.加入少量NaHSO4固体? D.加入少量CH3COONa固体
③在图2中分别画出常温下CH3COONa溶液和NaCN溶液中由水电离出的c(OH-)与其盐浓度的变化曲线.
(3)常温下,物质的量浓度相同的CH3COONa溶液和NaCN溶液中,CH3COONa溶液中各离子浓度之和______(填“>”、“<”或“=”)NaCN溶液中各离子浓度之和.
(4)已知:HCN(aq)
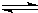
H+(aq)+CN-(aq)△H=+43.5kJ?mol-1
H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ?mol-1则NaCN在溶液中发生水解的热化学方程式:
CN-(aq)+H2O(1)
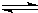
?HCN(aq)+OH-(aq)的△H=______.该反应25℃时的平衡常数K=______.
(需填具体数值,已知10-5.6=2.5×10-6)
2、填空题 (18分)
Ⅰ.(7分)次磷酸(H3PO2)是一种一元中强酸,具有较强的还原性。试回答下列问题:
(1)P的原子结构示意图为 ;
(2)NaH2PO2为 (填“正盐”或“酸式盐”),溶液中有关离子浓度从大到小的顺序为 。
(3)H3PO2可将溶液中的银离子还原为银单质,若氧化剂与还原剂的物质的量之比为4
3、选择题 从下列现象可以判断某一元酸是强酸的是( )
A.加热该酸至沸腾也不分解
B.该酸溶液可与石灰石反应放出CO2
C.该酸溶液可以溶解Al(OH)3沉淀
D.该酸溶液浓度为0.1mol/L时pH=1
4、选择题 与纯水的电离相似,液氨中也存在着微弱的电离: 2NH3 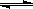 ?NH4++NH2-,据此判断以下叙述中错误的是:
?NH4++NH2-,据此判断以下叙述中错误的是:
A.液氨中含有NH3、NH4+、NH2-等微粒
B.一定温度下液氨中C(NH4+)・C(NH2-)是一个常数
C.液氨的电离到达平衡时C(NH3)=C(NH4+)=C(NH2-)
D.只要不加入其他物质,液氨中C(NH4+)=C(NH2-)
5、选择题 HClO是比H2CO3更弱的酸,反应Cl2+H2O HCl+HClO达到平衡后,要使HClO浓度增大可加入(?)
HCl+HClO达到平衡后,要使HClO浓度增大可加入(?)
A.NaOH
B.HCl
C.CaCO3
D.H2O