1、选择题 下列关于Al2O3的说法正确的是
[? ]
A.Al2O3也可以通过分解反应制得
B.Al2O3是两性氧化物
C.Al2O3非常致密,所以可用铝制容器盛盐酸和NaOH溶液等
D.擦去表面氧化铝的铝条,在酒精灯上灼烧时,熔化的铝纷纷滴落下来
2、选择题 进行化学实验,观测实验现象,通过分析推理得出正确的结论是化学学习的方法之一。下列对有关实验事实的解释正确的是
[? ]
A.SO2气体通入溴水(橙红色)褪色,表现了SO2的漂白性;足量的二氧化硫通入紫色石蕊试液中先变红后褪色,因为生成酸使其变红,又因为SO2的漂白性,使其褪色
B.浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸
C.常温下,将铝片放入浓硫酸中,无明显现象,说明铝不与冷的浓硫酸反应
D.向CuSO4溶液中加入一小块金属钠,则钠与Cu2+反应可置换出铜
3、填空题 (12分)从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
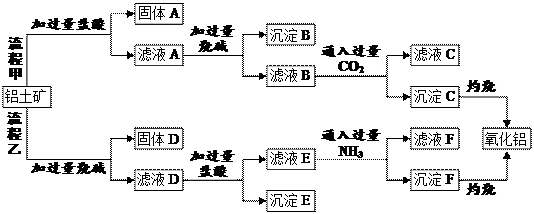
请回答下列问题:
⑴流程甲中,固体A的主要成分是______(填化学式,下同),沉淀B的主要成分是_______,生成沉淀C的离子方程式为__________________。
⑵流程乙中,加过量烧碱时发生反应的离子方程式为________________,沉淀E的主要成分是_________。
⑶生成沉淀F的离子方程式为____________________________________。
4、填空题 I、某同学设计实验将Fe3O4和CuO组成的混合物X进行如图所示的转化(每一步均反应完全)
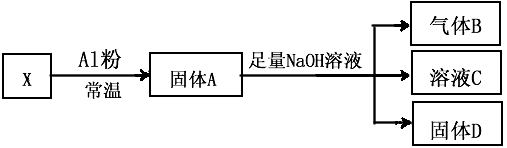
(1)生成气体B的化学方程式是____________________________。
(2)将固体D投入过量稀硫酸并充分反应后,过滤,再向滤液加入双氧水,得黄色溶液。 写出当加入双氧水时溶液中发生反应的离子方程式:________________________ 。
(3)若已知固体X的质量为7.2g反应中Al粉的质量是2.7g,气体B在标准状况下的体积为672mL,则固体D的质量是____________ g.
II、混合物A由碳酸钠和碳酸氢钠组成。现有两包质量相等的混合物A:
(4)若向其中一包加入100mL 3mol/L的Ba(OH)2溶液(过量),使HCO3-、CO32-全部变为沉淀,过滤后,再向滤液中加入200mL 2mol/L的稀盐酸,溶液恰好呈中性。
①写出下列反应的离子方程式
碳酸氢钠与过量氢氧化钡的反应:____________________________;
②混合物A中NaHCO3的质量为____________________g。
(5)若向另一包中先加50mL8mol/L的HCl溶液,使HCO3-、CO32-全部变为CO2后,再加50mL2mol/L的
Ba(OH)2溶液,混合后的溶液pH=14(混合后溶液体积变化忽略不计、在常温下)。混合物A中Na2CO3的质量为_______________g。
5、填空题 (13分)某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
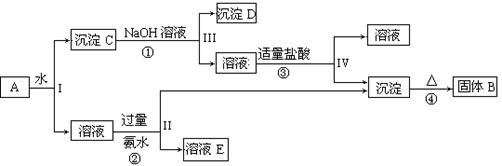
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是?。
(2)根据上述框图反应关系,写出下列B、 D所含物质的化学式
固体B?;沉淀D?。
(3)写出①、②反应的离子方程式:
①?;②?;
(4)以Fe2O3为原料,可制备FeCl2溶液,请写出有关的化学反应方程式,试剂任选。
?