1、选择题 下列说法正确的是
A.碳酸氢根离子的电离方程式: HCO3-+H2O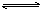 H3O++ CO32-
H3O++ CO32-
B.从上到下,卤族元素的非金属性逐渐减弱,故氢卤酸的酸性依次减弱
C.因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
D.NaCl晶体中每个Na+同时吸引着6个Cl-,CsCl晶体中每个Cl-同时吸引着6个Cs+
参考答案:A
本题解析:本题考查电离平衡、元素周期律及晶体结构知识;碳酸氢根,是弱酸酸式根,存在电离平衡,A正确;卤族元素从上到下,氢卤酸的酸性依次增强,B错误;非金属性强弱的判断,依据最高价氧化物对应水化物酸性强弱,HClO不是最高价含氧酸,不能做为判断的依据,C错误;CsCl晶体中每个Cl-同时吸引着8个Cs+,D错误。
本题难度:一般
2、选择题 下列判断正确的是?(? )
)
A.非金属氧化物一定是酸酐
B.酸酐一定是非金属氧化物
C.晶体中一定存在化学键
D.碱性氧化物一定是金属氧化物
参考答案:D
本题解析:略
本题难度:简单
3、填空题 科学家从化肥厂生产的(NH4)2SO4中检出组成N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以
SO42-和N4H44+两种离子形式存在,植物的根系极易吸收N4H44+,但它遇到碱时,会生成一种类似白磷的N4分子,N4分子不能被植物吸收。请回答下列问题:
(1)N4和N2的关系正确的是___________(填序号);
A.同种单质 B.同位素 C.同分异构体 D.同素异形体
(2)N4H4(SO4)2______ (填“能”或“不能”)和草木灰混合施用;
(3)已知白磷、NH4+、N4H44+的空间构型均为四面体,NH4+的结构式为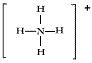 (→表示共用电子对由N原子单方面提供),白磷(P4)的结构式为
(→表示共用电子对由N原子单方面提供),白磷(P4)的结构式为 。请画出N4H44+的结构式__________________。
。请画出N4H44+的结构式__________________。
(4)已知液氨中存在着平衡2NH3 NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:______________________
NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:______________________
参考答案:(1)D
(2)不能
(3)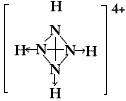 ?
?
(4)8NH3+4CsOH==N4+4CsNH2+6H2↑+4H2O
本题解析:
本题难度:一般
4、选择题 根据下表给出的几种物质的溶沸点数据,判断下列说法中错误的是?(?)?
?
| NaCl
| MgCl2
| AlCl3
| SiCl4
| 单质B
|
熔点/℃
| 810
| 710
| 180
| -68
| 2300
|
沸点/℃
| 1465
| 1418
| 160
| 57
| 2500
|
A、SiCl4是分子晶体;? B、单质B可能是原子晶体;
C、AlCl3加热能升华;? D、NaCl 比MgCl2更易熔化
参考答案:D
本题解析:氯化钠的熔点高于氯化镁的熔点 ,所以MgCl2比NaCl更易熔化,D不正确;四氯化硅的熔沸点很低,因此是分子晶体;单质B的熔沸点很高,因此可能是原子晶体;氯化铝的沸点高于氯化铝的熔点,则氯化铝加热能升华,答案选D。
点评:该题是高考中的常见题型和考点,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和解题方法的指导与训练。该题的关键是记住晶体类型的含义以及判断的依据,并能结合题意灵活运用即可,有利于培养学生的创新思维能力和逻辑推理能力。
本题难度:简单
5、选择题 下列式子中,真实表示物质分子组成的是?(?)
A.H2O
B.NH4Cl
C.SiO2
D.C
参考答案:A
本题解析:略
本题难度:简单