1、选择题 下列各组中两种浓溶液相混合时既无沉淀析出又无气体放出的是
A.Ba(HCO3)2、NaHSO4
B.NaHCO3、Al2(SO4) 3
3
C.Mg(HCO3)2、CaCl2
D.Na2SiO3、HCl
参考答案:C
本题解析:略
本题难度:一般
2、简答题 下表为元素周期表的一部分,请参照①~⑩在表中的位置,用化学用语回答下列问题:
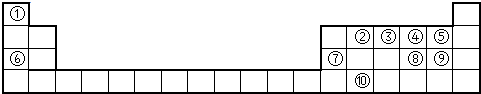
(1)元素③形成的单质的电子式为______;元素②形成的最高价氧化物的结构式为______.
(2)⑥、⑦两元素的最高价氧化物的水化物之间反应的离子方程式为______.
(3)②、③、④、⑤元素形成的氢化物中,热稳定性最强的是______(填化学式),沸点最高的是______(填化学式).
(4)⑧、⑨元素的最高价氧化物的水化物酸性强弱比较______(填化学式).
(5)元素⑩在周期表中的位置______;该元素的单质主要用途______(选填一种).
参考答案:(1)表中③是N,N2的电子式是

;②是C,其最高氧化物是CO2,其结构式为O=C=O,故答案为:

;O=C=O;
(2)⑥、⑦分别是Na、Al,其最高价氧化物的水化物分别是NaOH和Al(OH)3,二者反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(3)②、③、④、⑤分别是C、N、O、F,根据同周期从左到右元素氢化物稳定性逐渐增强可知,稳定性最强的是HF,沸点最高的应该是H2O,因为在这几种元素的氢化物中只有H2O在常温下是液体,其余是气体(也可从氢键解释),故答案为:HF;H2O;
(4)⑧、⑨分别是S、Cl,根据同周期最高价氧化物的水化物从左到右酸性逐渐增强可知,酸性为:HClO4>H2SO4,故答案为:HClO4>H2SO4;
(5)⑩是Ge,处于周期表中的第4周期ⅣA族,与Si一样可做半导体材料,故答案为:第4周期ⅣA族;半导体材料.
本题解析:
本题难度:一般
3、选择题 下列操作中,溶液的颜色不发生变化的是
A.氯化铁溶液中加入足量铁粉,充分振荡
B.氯化铁溶液中滴加硫氰化钾(KSCN)溶液
C.氧化铜固体加入稀盐酸中,完全溶解
D.碳酸氢钠溶液中滴加稀盐酸
参考答案:D
本题解析:A、氯化铁为黄色溶液,与铁反应生成氯化亚铁为浅绿色;
B、三价铁离子与硫氰根显血红色;
C、盐酸无色,反应生成氯化铜为蓝色。
本题难度:简单
4、选择题 不定项
x、y、z为短周期元素,z原子最外层电子数等于x、y原子最外层电子数之和,且z-离子比x的阳离子多三个电子层。下列推断不符合事实的是
A.y的离子半径一定大于z的离子半径
B.x、y都是非金属元素
C.y与z原子间只能形成分子晶体
D.y的氢化物沸点可能比z的氢化物沸点高
参考答案:A
本题解析:
本题难度:简单
5、选择题 下列有关物质性质的比较正确的是
[? ]
A.同主族元素的单质从上到下,非金属性减弱,熔点增高
B.主族元素正化合价数,等于它的族序数
C.元素的非金属性越强,它的气态氢化物水溶液的酸性越强
D.酸性:HClO4>H2SO4>H3PO4>H2SiO3
参考答案:D
本题解析:
本题难度:一般