1、选择题 实验室需配制一种强酸溶液500mL,c(H+)=2mol/L,下列配制方法可行的是
A.取100mL5mol/ LH2SO4,加入400mL水
LH2SO4,加入400mL水
B.取200mL5mol/LHCl,加水稀释至500mL
C.取100 mL 5mol/LH2SO4,加500mL水稀释
5mol/LH2SO4,加500mL水稀释
D.取100 mL5mol/LHNO3,加水稀释至500mL
参考答案:B
本题解析:略
本题难度:简单
2、填空题 (7分)已知“84消毒液”的有效成分是NaClO。试根据所学知识完成下列问题。
(1)试以食盐、水为原料,设计实验室制取“84消毒液”。(已知电解食盐水可得到氯气、氢氧化钠、水)
①实验内容为:电解食盐水制得氯气;
②实验内容为:?;
反应方程式为:?
③将制得的溶液装瓶保存。
(2)“84消毒液”的消毒原理是(用化学方程式表示)?。用于杀死病菌的成分是?(写化学式)。
参考答案:(7分)(1)②将Cl2通入NaOH(aq)中(2分) ,2NaOH+Cl2===NaCl+NaClO+H2O(2分) (2 )2NaClO+H2O+CO2===Na2CO3+2HClO(2分) ;HClO(1分)
)2NaClO+H2O+CO2===Na2CO3+2HClO(2分) ;HClO(1分)
本题解析:略
本题难度:一般
3、填空题 (7分)有一无色混合气体可能是由HCl、NO、NO2、CO2、NH3、H2中的一种或几种混合而成,将此气体通过盛有浓H2SO4时的洗气瓶时,气体体积减小。继续通过装有过氧化钠的干燥管,发现从出气口出来的气体显红棕色,再将该气体全部通入盛满水倒立于水槽中的试管内,发现最后试管里仍为一满试管液体.由此可推知原气体中一定存在__________? ____,一定不存在__________? _ ____,由最终结果可知原气体中________? _ 气体的体积比为?
参考答案:(7分)一定存在NH3? NO? CO2,(2分,错填不得分)
一定不存在NO2? HCl? H2 ?,(2分,错填不得分)
由最终结果可知原气体中NO? CO2?气体的体积比为2:3?(共3分)
本题解析:略
本题难度:一般
4、实验题 某学生利用以下装置探究喷泉实验。其中A、F分别为硫化氢和氯气的发生装置,C为纯净干燥的氯气与硫化氢反应的装置。
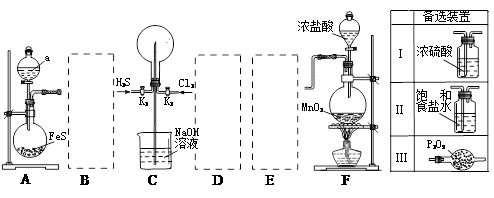
请回答下列问题:
(1)装置F中发生反应的化学方程式?。
(2)装置A中的分液漏斗内液体a可选用?(选填以下选项的代号)
A.盐酸? B.浓硫酸? C.稀硫酸? D.稀硝酸
(3)虚线框内应添加必要的除杂装置,请从上图的“备选装置”中选择合适装置的编号,填入下列空格。B__________、D__________、E__________。
(4)打开K1、K2,将常温压下的H2S、Cl2以体积比1:1充满烧瓶后,烧瓶中发生的反应用化学方程式表示为?;关闭K1、K2,始终看不到烧瓶内产生“喷泉”现象,理由是:?。
(5)在操作(4)的基础上,引发喷泉操作方法是?。
参考答案:(1)(共3分)MnO2 + 4HCl(浓)  MnCl2 + Cl2↑ + 2H2O?
MnCl2 + Cl2↑ + 2H2O?
(2)(共2分)AC
(3)(共3分)Ⅲ、Ⅰ、Ⅱ
(4)(共5分)H2S+Cl2=2S+2HCl;(3分,化学式2分,配平1分)?烧瓶内的气压与外界气压相同(1分),不能产生压强差,故无喷泉现象(1分)。
(5)(共3分)方法① 用手(或热毛巾)将烧瓶捂热或将烧瓶微热(1分),烧瓶内气体受热膨胀(即增大压强,1分),使HCl与烧杯中溶液接触,即可引发喷泉(1分);
方法② 用冰水或其它制冷剂浇在烧瓶上(给烧瓶降温,1分),以减小烧瓶内气体的压强,(1分)烧杯中溶液通过导管进入烧瓶内与HCl气体接触,即可引发喷泉(1分)。
本题解析:
△
?试题分析:(1)装置F为制取氯气的发生装置,所以发生的反应方程式为:MnO2 + 4HCl(浓) ="==" MnCl2 + Cl2↑ + 2H2O 。
(2)装置A为制取H2S的发生装置,利用强酸和硫化物反应制得,但是硫化物中的S有较强还原性,不能用强化性的酸制备,所以不能用浓硫酸、稀硝酸,故选AC。
(3)虚线框B为H2S气体的干燥装置,不能用强氧化性的的浓硫酸干燥,所以选五氧化二磷装置Ⅲ;虚线框D、E分别为氯气的除杂装置和干燥装置,D用装置Ⅱ饱和食盐水可以除去杂质HCl,用装置Ⅰ浓硫酸可以除去水蒸气。
(4)H2S、Cl2以体积比1:1充满烧瓶,则发生的氧化还原反应按照1:1反应,所以方程式为:H2S+Cl2=2S+2HCl。观察方程式可得知反应中前后气体系数不变,所以反应前后气体压强不变,烧瓶内的气压与外界气压相同,不会造成压强差,不能形成喷泉。
(5)要使上述实验产生喷泉现象,必须要让烧瓶内的气压和外界气压产生压强差,所以可以采取升温或冷却的方法:方法① 用手(或热毛巾)将烧瓶捂热或将烧瓶微热,烧瓶内气体受热膨胀,使HCl与烧杯中溶液接触,即可引发喷泉;方法② 用冰水或其它制冷剂浇在烧瓶上,以减小烧瓶内气体的压强,烧杯中溶液通过导管进入烧瓶内与HCl气体接触,即可引发喷泉
本题难度:一般
5、填空题 已知稀的酸与稀的碱发生中和反应,生成1mol水所放出的热叫中和热,用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是?。
(2)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量??(填“相等、不相等”),所求中和热?(填“相等、不相等”),
(3)已知滇池中学高二一班某同学的实验记录如下,
实验次数
| 酸的温度
| 碱的温度
| 反应最高温度
|
1
| 21.5℃
| 20.5℃
| 24.3℃
|
2
| 21.5℃
| 21.5℃
| 25.0℃
|
3
| 16.0℃
| 18.5℃
| 21.5℃
|
请根据有用数据计算中和热(酸碱的密度均视为1g/ml, C=4.17J/g.℃)?
(4)用相同浓度和体积的氨水(NH3・H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会?;(填“偏大”、“偏小”、“无影响”)。
参考答案:(1)环形搅拌器?(2)不相等;相等(3)△H=" -56.7KJ/mol" ?(4)?偏小
本题解析:(1)在反应过程中为了使溶液混合均匀,需要搅拌,因此从实验装置上看,图中尚缺少的一种玻璃用品是环形搅拌器。
(2)改变酸或碱的用量,反应中实际放出的热量是不同,但中和热是不变的。
(3)根据表中数据可知,1、2、3实验中温度差值分别是24.3℃-(21.5℃+20.5℃)÷2=3.3℃、25.0℃-(21.5℃+21.5℃)÷2=3.5℃、21.5℃-(16℃+18.5℃)÷2=4.25℃.显然第三实验的误差大,舍去,即温度变化的平均值是3.4℃。反应中生成水的物质的量是0.025mol,所以该反应的中和热是△H=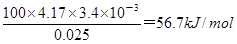 。
。
(4)由于一水合氨是弱电解质,存在电离平衡,电离是吸热的,所以用相同浓度和体积的氨水(NH3・H2O)代替NaOH溶液进行上述实验,测得的中和热的数值偏小。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,主要是考查学生对中和热测定的了解掌握程度,有利于培养学生规范严谨的实验设计能力,提高学生的应试能力和学习效率。该类试题主要是以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
本题难度:一般