1、选择题 通过化学反应不能实现的是(?)
A.生成一种新离子
B.生成一种新分子
C.生成一种新原子
D.生成一种新单质
参考答案:C
本题解析:原子是化学变化中的最小微粒,所以通过化学反应不可能生成一种新原子,选项C是错误的,其余都是正确的,答案选C。
本题难度:简单
2、填空题 已知和碳元素同主族的X元素位于周期表中的第一长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们所形成化合物的分子式是XY4。试回答:
(1)X元素的原子基态时电子排布式为?;Y元素原子最外层电子的轨道表示式为?。
(2)若X、Y两元素电负性分别为1.8和3.0,则XY4中X与Y之间的化学键为?(填“共价键”或“离子键”)。
(3)该化合物的空间结构为?,中心原子的杂化类型为?,分子为?(填“极性分子”或“非极性分子”)。
(4)该化合物在常温下为液体,该化合物中分子间作用力是?。
(5)该化合物的沸点与SiCl4比较,?(填化学式)的较高,原因是?。
参考答案:(1)1s22s22p63s23p63d104s24p2?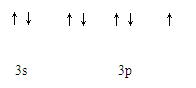 ?
?
(2)共价键
(3)(3分)正四面体形? sp3杂化?非极性分子
(4)范德华力
(5)GeCl4?二者结构相似,GeCl4相对分子质量大,分子间作用力强,沸点高
本题解析:略
本题难度:一般
3、选择题 已知R、M、T、G、J为原子序数依次增大且相邻的同一短周期主族元素。下列说法一定正确的是
A.若R、M的最高价氧化物的水化物是碱,则M(OH)n+1的碱性比R(OH)n的碱性强
B.若T(OH)n为两性氢氧化物,则J元素形成的单质存在同素异形现象
C.若J的氢化物是常见的强电解质,则M单质是光导纤维的主要成分
D.若M的最高正价为+4,则五种元素全是非金属元素
参考答案:B
本题解析:本试题考查了短周期中,元素周期律在周期表中的递变规律及少部分原理知识,主要是金属性及非金属性递变性的考查。对于此类试题,主要先找出所给元素在周期表中的位置关系,然后结合已经学习的金属性及非金属性的递变规律来解题。题中,五种元素为同一周期且原子序数依次增大且相邻,也就是说,是周期表中连续的五种元素,只要知道其中一种,其他都能推断出来。A选项,同周期从左向右,金属性减弱,碱性减弱;B选项,T为铝,J为磷,红磷与白磷互为同素异形体,正确。C选项,J为Cl,M为硅,光导纤维的主要成分为二氧化硅而不是硅单质;D选项,M最高价+4,当处于第三周期时,R为金属铝。
本题难度不大,主要是考查学生对短周期元素的熟练程度
本题难度:一般
4、选择题 短周期元素中,原子基态时具有1个未成对电子的元素共有多少种(?)
A.5
B.6
C.7
D.8
参考答案:C
本题解析:短周期元素中,原子基态时具有1个未成对电子的元素的最外层电子排布符合ns1、np1、np5的特点,n=1时,1种;n=2时3种;n=3时3种,共7种,答案选C。
本题难度:一般
5、选择题 下列各组性质的比较中正确的是

A.酸性: HClO4<HBrO4<HIO4
B.碱性强弱: KOH > NaOH > LiOH

C.稳定性: PH3>H2S>H Cl
D.氧化性: I2>Br2>Cl2
参考答案:B
本题解析:A错误,最高价含氧酸酸性随中心元素的非金属性增强而增强,所以正确的应该是
HClO4〉HBrO4〉HIO4
B正确,碱性强弱与金属的金属性有关,金属性越强,其形成的碱,碱性越强。
C错误,氢化物稳定性与元素的非金属性有关,非金属性越强,氢化物越稳定,HCl是三种物质中最稳定的。
D错误,正确的为:Cl2>Br2>I2
本题难度:一般