1�������� �� 300mL 2mol/L H2SO4��Һ�У�
��1��SO42-�����ʵ���Ũ���Ƕ��٣�
��2��H+�����ʵ���Ũ���Ƕ��٣�
��3�����ʵ������Ƕ��٣�
��4������Һ�к�H+�����ʵ����Ƕ��٣�
��5�����к��ж��ٸ�SO42-��
�ο��𰸣��⣺
��1��c(SO42-)= c(H2SO4)= 2mol/L
��2��c(H+)= 2c(H2SO4)= 4mol/L
��3�����ʼ�H2SO4��n (H2SO4)=c(H2SO4) ��V=2mol/L��0.3L= 0.6mol
m(H2SO4)=n(H2SO4)��M=0.6mol��98g/mol=58.8g
��4��n(H+)= 2n(H2SO4)= 1.2mol
��5��n(SO42-)=n(H2SO4)=0.6mol
N(SO42-)= n(H2SO4) ��NA= 0.6mol��6.02��1023mol-1=3.612��1023
���������
�����Ѷȣ�һ��
2�������� ����50mL�ܶ�Ϊ1.18g/mL����������Ϊ36.5%��Ũ�����
��1����Ũ��������ʵ���Ũ��
��2������Ũ����������ˮϡ����200mL����ϡ�ͺ���������ʵ���Ũ��Ϊ���٣�
�ο��𰸣���1���������������ʵ���Ũ�ȵĹ�ϵΪ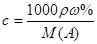 �����Ը������Ũ��Ϊ
�����Ը������Ũ��Ϊ
 ��
��
��2��50mlϡ����200ml��˵��ϡ����4��������ϡ���������ʲ����֪��ϡ�ͺ��Ũ��Ϊ ��
��
����������������ʵ���Ũ�ȵ��йؼ��㡣�������������ʵ���Ũ�ȶ�����������ʾ��Һ����ɣ�����֮��Ĺ�ϵΪ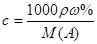 ����ϡ���������ʵ����ʵ����Dz���ģ��ݴ˿�����ʽ���㡣
����ϡ���������ʵ����ʵ����Dz���ģ��ݴ˿�����ʽ���㡣
�����Ѷȣ�һ��
3������� ���Ṥҵ�����е�β�����ô�����Һ���գ��йصĻ�ѧ��ӦΪ��
2NO2 + Na2CO3 �� NaNO2 + NaNO3 + CO2��?��
NO + NO2 + Na2CO3 �� 2NaNO2 + CO2������������
�Ÿ��ݷ�Ӧ�٣�ÿ����22.4L����״���£�CO2������Һ����������___________g��
������1000g��������Ϊ21.2%�Ĵ�������Һ����Na2CO3��10H2O?g��
������1000g��������Ϊ21.2%�Ĵ�������Һ���������Ṥҵβ����ÿ����22.4L����״���£�CO2ʱ������Һ����������44g��
������Һ��NaNO2��NaNO3�����ʵ���֮��?
�� 1000g ��������Ϊ21.2%�Ĵ�����20�澭����������Ṥҵβ����������688gˮ����ȴ��0�棬��������NaNO2?�ˣ�0��ʱ��NaNO2���ܽ��Ϊ71.2g/100gˮ��?
�ο��𰸣���48��2�֣���m(Na2CO3��10H2O) = 572g��2�֣�
�Ǣ�n(NaNO2)��n(NaNO3)=5��3��2�֣�
��������m(NaNO2)(���) =172.5g��71.2g=101.3g?��2�֣�
����������Ÿ��ݷ�Ӧ��ÿ����22.4L����״���£�CO2��������2molNO2����������Һ����������2��46g��44g��48g��
(2)1000g ��������Ϊ21.2%�Ĵ�����Һ��̼���Ƶ�������212g�����ʵ�����2mol��������ҪNa2CO3��10H2O��������2mol��286g/mol��572g��
��3����������Һ��NaNO2��NaNO3�����ʵ����ֱ���x��y����Ӧ��������Һ���ӵ�������48y���ڷ�Ӧ�������ɵ�����������x��y����������Һ���ӵ�������16��x��y������16��x��y����48y��44������Ϊy����x��y��/2=1,���x��5/4��y��3/4����������Һ��NaNO2��NaNO3�����ʵ���֮��5�U3��
�ڸ��ݢٿ�֪����Ӧ����Һ��������1088g����������������2.5mol����������1.5mol��������Һ����������127.5g������������172.5g�������ܼ�ˮ��������788g��������688gˮ��ʣ��ˮ��100g�������������������172.5g��71.2g="101.3g" ��
�����Ѷȣ�һ��
4��ѡ���� ���и��������У�ԭ������ͬ����( )
A��2 L CO��2 L O2
B����״����2 mol CO2��44.8 Lˮ
C��0.2 mol H2��4.48 L HCl
D��ͬ��ͬѹ�£�2L������2L�������Ȼ���Ļ����