1、填空题 某温度下,在2 L的密闭容器中,X、Y、Z三种物质随时间变化的曲线如图所示。
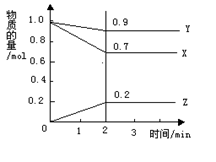
由图中数据分析:该反应的化学方程式为:?。反应开始至2 min ,Z的平均反应速率为?。
2、选择题 可逆反应2NO2(g)?2NO(g)+O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n?molO2的同时生成2n?mol NO2
②单位时间内生成n?molO2的同时生成2n?mol NO
③NO2、NO、O2的物质的量浓度比值为2:2:1
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的总压强不再改变的状态.
A.①④⑥
B.②③⑤
C.①③④
D.全部
3、选择题 甲酸甲酯水解反应方程武为:HCOOCH3(aq)+H2O(l) HCOOH(aq)+CH3OH(aq) △H>0。某温度下,VL溶液中各组分的起始量如下表,HCOOCH3转化率随反应时间(t)的变化如下图(假设溶液体积不变),下列说法正确的是
HCOOH(aq)+CH3OH(aq) △H>0。某温度下,VL溶液中各组分的起始量如下表,HCOOCH3转化率随反应时间(t)的变化如下图(假设溶液体积不变),下列说法正确的是

A.温度升高,该反应的平衡常数减小
B.0?10min,HCOOCH3的平均反应速率 u="0." 003mol・L-1 ? min-1
C.HCOOCH3平均反应速率先是增大,后减小,最后保持不变
D.80min时,反应刚达平衡,反应物转化率保持不变
4、填空题 已知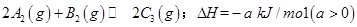 ,在一个有催化剂的固定容积的容器中加入2mol
,在一个有催化剂的固定容积的容器中加入2mol 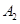 和1mol
和1mol 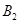 ,在500℃时充分反应达平衡后
,在500℃时充分反应达平衡后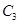 的浓度为w mol/L,放出热量b kJ。
的浓度为w mol/L,放出热量b kJ。
(1)比较a______b(填>、=、<)
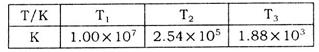
(2)下表为不同温度下该反应的平衡常数。由此可推知,表中 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
若在原来的容器中,只加入2mol 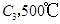 时充分反应达平衡后,吸收热量ckJ,
时充分反应达平衡后,吸收热量ckJ,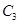 的浓度________(填>、=、<)w mol/L。
的浓度________(填>、=、<)w mol/L。
(3)在相同条件下要想得到2akJ热量,加入各物质的物质的量可能是
A.4mol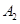 和2mol
和2mol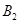 ? B.4mol
? B.4mol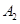 、2mol
、2mol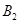 和2mol
和2mol 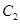
C.4mol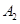 和4mol
和4mol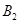 ? D.6mol
? D.6mol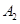 和4mol
和4mol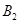 ?
?
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是___________。
A.及时分离出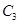 气体? B.适当升高温度
气体? B.适当升高温度
C.增大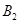 的浓度?D.选择高效的催化剂
的浓度?D.选择高效的催化剂
5、选择题 工业制取硫酸有一步重要反应是SO2在400~500℃下的催化氧化,2SO2+O2

2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述有关说法中错误的是( )
A.使用催化剂是为了加快反应速率,提高生产效率
B.在上述条件下,SO2不可能100%的转化为SO3
C.达到平衡时,SO2的浓度与SO3的浓度相等
D.为了提高SO2的转化率,应适当提高O2的浓度