1、填空题 (10分)在一定条件下,xA + yB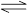 zC,达到平衡,试填写下列空白:
zC,达到平衡,试填写下列空白:
( 1 ) 若A、B、C都是气体,减压后向逆反应方向移动,则x、y、x之间的关系是? ?。
( 2 ) 已知C是气体,且x+y=z,加压时平衡如果发生移动,则平衡必向? ?方向移动,且A、B的状态中至少有一种是___________________。
( 3 ) 若B、C是气体,其他条件不变时增加A的用量,平衡不移动,则A的状态为? ?。
( 4 ) 加热后C的百分含量减少,则正反应是?反应(选填“吸热”、“放热”)。
参考答案:(每空2分,共10分)
(1)x+y>z(2)逆反应,固态或液态?(3)固态或液态?(4)放热
本题解析:略
本题难度:一般
2、选择题 在2A(g)+B(g)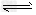 3C(g)+4D(l)中,表示该反应速率最快的是?
3C(g)+4D(l)中,表示该反应速率最快的是?
[? ]
A.?υ(A)?=?0.5mol・L-1・s-1?
B.?υ(C)?=?0.8mol・L-1・s-1 ?
C.?υ(B)?=?0.3mol・L-1・s-1?
D.?υ(D)=?1.8mol・L-1・s-1
参考答案:C
本题解析:
本题难度:简单
3、选择题 在t℃时,将0.2 mol X和0.8 mol Y充入体积恒定的密闭容器中,当反应X(g)+Y(g) 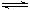 nZ(g)+R(g)达到平衡时,若将反应混合气体中各物质浓度均增大一倍,X的转化率不变,已知t℃时该反应的K=1,则X的转化率为
nZ(g)+R(g)达到平衡时,若将反应混合气体中各物质浓度均增大一倍,X的转化率不变,已知t℃时该反应的K=1,则X的转化率为
A.80%
B.65%
C.45%
D.37%
参考答案:A
本题解析:略
本题难度:一般
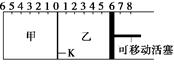
4、选择题 如图,隔板K可左右移动,甲中充入2 mol A和1 mol B,乙中充入2 mol C和1 mol He,此时K停在0处。发生反应2A(g)+B(g)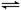 2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是
2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是
A.达平衡后,隔板K最终停留在左侧刻度0~2之间
B.若平衡时K停留在左侧1处,则活塞停留在右侧6处
C.达到平衡时,甲容器中B的物质的量小于于乙容器中B的物质的量
D.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
参考答案:B
本题解析:反应是体积减小的可逆反应,所以在反应过程中乙中气体的物质的量增加,甲中气体的物质的量减少,因此K向作移动。由于是可逆反应,所以甲中气体的物质的量一定大于2mol,因此隔板K最终停留在左侧刻度0~2之间,A正确。乙容器相当于在甲容器的基础上,平衡时通入稀有气体,在压强不变的情况下,平衡向生成A、B的方向移动,所以选项C正确。当K不再滑动时,说明反应达到平衡状态,D正确。若平衡时K停留在左侧1处,则乙中气体的物质的量变化量大于1个单位,所以B不正确,答案选B。
本题难度:一般
5、填空题 (16分)为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇。“绿色自由”构想的部分技术流程如下:
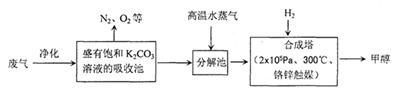
合成塔中反应的化学方程式为?;△H<0。从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,除考 虑温度对反应速率的影响外,还主要考虑了?。
虑温度对反应速率的影响外,还主要考虑了?。
从合成塔分离出甲醇的原理与下列?操作的原理比较相符(填字母)。
A.过滤
B.分液
C.蒸馏
D.结晶