1��ѡ���� ij�¶�ʱ��BaSO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ����
(��ʾ��BaSO4(s)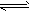 Ba2+(aq)��SO42-(aq)��ƽ�� ����Ksp��c(Ba2+)��c(SO42-)����Ϊ�ܶȻ�����)
Ba2+(aq)��SO42-(aq)��ƽ�� ����Ksp��c(Ba2+)��c(SO42-)����Ϊ�ܶȻ�����)
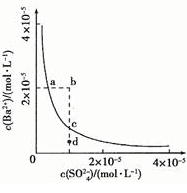
[? ]
A������Na2SO4����ʹ��Һ��a��䵽b��
B��ͨ����������ʹ��Һ��d��䵽c��
C��d����BaSO4��������
D��a���Ӧ��Ksp����c���Ӧ��Ksp
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� ��һ���¶��£���Mg(OH)2������ˮ��Һ�дﵽ����ƽ��ʱ��Mg(OH)2(s)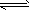 Mg2++2OH-����ʹ����Mg(OH)2�������٣���c(Mg2+)���䣬�ɲ�ȡ�Ĵ�ʩ��
Mg2++2OH-����ʹ����Mg(OH)2�������٣���c(Mg2+)���䣬�ɲ�ȡ�Ĵ�ʩ��
[? ]
A����MgCl2
B����H2O
C����NaOH
D����HCl
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3��ѡ���� ��һ���¶��£��Ȼ���������Һ��C(Ag+)��C(Cl-) = Ksp���ֽ�����AgCl����ֱ�������������У�������Һ��AgCl���ܽ��������
��.20ml 0.1mol/LHCl��Һ?��B.30ml 0.2mol/LHCl��Һ
C.40ml����ˮ?����D.50ml 0.05mol/LNaCl��Һ
�ο��𰸣�C
�����������Ũ�Ȼ���֪����Һ�е�c(Cl-)Խ��AgCl���ܽ��ԽС������ѡ���е�c(Cl-)����Ϊ��0.1mol/L��0.2mol/L��0��0.05mol/L����ѡ��C��������
�����Ѷȣ�һ��
4������� ��1��100��ʱ��ˮKw=1��10-12?mol2?L-2�ڸ��¶��£���1mL?0.001mol?L-1��NaOH��Һ��pHΪ______������ˮϡ����100L������Һ��pHΪ______��
��2�������£�pH=1��ϡ����a?L��pH=12�Ŀ�����b?L��Ϻ���Һ��pH=2��������Һ���ǰ������仯����a��b=______��
��3����֪25��ʱ100gˮ������0.74g��Ca��OH��2���ﵽ���ͣ����������Ca��OH��2���ӻ�ΪKsp=______��
�ο��𰸣���1��1mL?0.001mol?L-1��NaOH��Һ��c��OH-��=c��NaOH��=1��10-3mol/L������c��H+��=10-121��10-3mol/L�T1��10-9mol/L�����Ը���Һ��pH=-lg��1��10-9��=9����1mL?0.001mol?L-1��NaOH��Һ����ˮϡ����100L��NaOH��Һ��c��OH-����1��10-6mol/L�����Ը���Һ��pH=-lg��1��10-6��=6���Գʼ��ԣ��ӽ����ԣ�
�ʴ�Ϊ��9�� 6��
��2�������£�pH=1��ϡ����c��H+��=0.1mol/L��pH=12�Ŀ�����c��OH-��=c��NaOH��=0.01mol/L��Ҫʹ�û�Ϻ���ҺpH=2�����Ϻ�0.1a-0.01ba+b=0.01mol/L����ab=2��9��
�ʴ�Ϊ��2��9��
��3��25��ʱ100gˮ������0.74g��Ca��OH��2���ﵽ���ͣ����������100��ˮ���ܽ�0.74��Ca��OH��2�����ʵ���Ϊ0.01mol����ʱ��Һ������100.74�ˣ���Һ�����100.74g��1g/cm3=100.74mL����ʱCa��OH��2���ʵ���Ũ��Ϊ��C=nV=0.01mol0.10074L=0.099mol/L�����ԣ���ʱCa2+���ʵ���Ũ��Ϊ��0.099mol/L��OH-���ʵ���Ũ��Ϊ��0.198mol/L��Ksp=c��Ca2+����c��OH-��2=0.004 mol3?L-3��
�ʴ�Ϊ��0.004 mol3?L-3��
���������
�����Ѷȣ�һ��
5��ѡ���� ����˵������ȷ���ǣ�������
A��Kspֻ�����ܵ���ʵ����ʺ��¶��й�
B������Ksp��ZnS����Ksp��CuS��������ZnS������һ�������¿�ת��ΪCuS����
C�������������䣬����Ũ�ȸı�ʱ��Ksp����
D���������ܵ���ʣ�KspС�ģ��ܽ��һ��С
�ο��𰸣�A����ѧ��Ӧƽ�ⳣ��ֻ�뷴Ӧ���������ʺ��¶��йأ���������ȷ��ʱ��ֻ���¶��й��ˣ���A��ȷ��
B������Ksp��ZnS����Ksp��CuS������ZnS������Һ�м���Cu2+��Һ��������CuS��������B��ȷ��
C��Kspֻ���¶ȵ�Ӱ�죬��Ũ���أ���C��ȷ��
D���������������ӵĸ�������ͬ��ͬһ���͵����ܵ���ʣ�Ksp����ֵԽ�����ܵ������ˮ�е��ܽ�����Խǿ���ܽ��Խ�������������ӵĸ����Ȳ�ͬ�����ܵ���ʣ�����ֱ����Ksp�Ĵ�С�Ƚ����ǵ��ܽ�����������ͨ��������бȽϣ���D����
��ѡD��
���������
�����Ѷȣ�һ��