1、填空题 (4分)工业制备氯化铜时,将浓盐酸加热至80 ℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液,采用以下步骤[参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3]。请回答以下问题:
(1)第一步除去Fe2+,有人用强氧化剂NaClO将Fe2+氧化为Fe3+:
①加入NaClO后,溶液的pH变化是 (填代号)。
A.一定增大 B.一定减小 C.可能增大 D.可能减小
②你认为用NaClO作氧化剂是否妥当? (填“是”或“否”),理由是 。
(2)除去溶液中Fe3+的方法是调整溶液的pH=3.7,现有下列试剂均可以使强酸性溶液的pH调整到3.7,可选用的有 。(多选)
A.NaOH
B.氨水
C.Cu2(OH)2CO3
D.Na2CO3
E.CuO
F.Cu(OH)2
2、选择题 下述根据下列操作和现象,所得结论正确的是
| 实验操作及现象
| 实验结论
|
A
| 分别向2mL0.1mol・L-1CH3COOH溶液和2mL0.1mol・L-1H3BO3溶液中滴加等浓度的NaHCO3溶液,前者有气泡产生,后者无明显现象
| 酸性:CH3COOH>H2CO3>H3BO3
|
B
| 向浓度均为0.1mol・L-1NaCl和NaI混合溶液中滴加少量AgNO3溶液,产生黄色沉淀
| 溶度积:Ksp(AgCl)<Ksp(AgI)
|
C
| 向无水乙醇中加入浓H2SO4,加热,产生的气体通入酸性KMnO4溶液,紫色褪去
| 证明生成了乙烯
|
D
| 将少量的溴水滴入NaI溶液中,再滴加CCl4,振荡、静置,溶液分为两层:上层溶液无色,下层溶液紫红色
| 氧化性:Br2>I2
|
3、选择题 已知:CaC2O4沉淀的Ksp=2.3×10-9,将等体积的CaCl2溶液与Na2C2O4溶液混合,若起始CaCl2的浓度为1×10-2mo1?L-1,则生成沉淀所需Na2C2O4溶液的最小起始浓度为( )
A.2.3×10-7mol?L-1
B.4.6×10-7mol?L-1
C.9.2×10-7mol?L-1
D.
×10-3mol?L-1
4、选择题 下表列出了几种常见物质的电离常数或溶度积

在一定量的0.2 mol/L CaCl2溶液中加入等体积的下列溶液,可以产生沉淀的是
[? ]
A.由水电离出的c(H+) =10-9mol/L的HF溶液
B.pH=10的氨水
C.1 mol/L的NaHCO3溶液
D.10-9 mol/L的AgNO3溶液
5、填空题 炼锌厂产生的工业废渣――锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4・7H2O和金属镉(Cd)是一个有益的尝试,其流程如下:
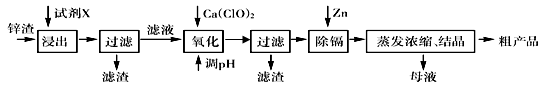
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7。试回答下列问题:
(1)浸出时用到的试剂X为?, 写出溶解过程中加快浸出速率和提高浸出率的两点措施:_______________________________,______________________________。
(2)写出加入Ca(ClO)2反应的离子方程式?。
(3)调节pH过程可以选用?(填“ZnO”或“NaOH”);本流程的pH调节一般调至5,其目的是??。
(4)写出过滤后加入过量的锌粉反应的离子方程式?。
(5)在蒸发浓缩操作时,要采取实验措施是:?。