1��ѡ���� Ԫ����������ԭ�ӽṹ���۳��ֵ����
A.ǰ�ߴ�
B.���ߴ�
C.���
D.����ȷ��
�ο��𰸣�B
���������Ԫ������������1869�����Ž��з�����ģ�ԭ�ӽṹ��������1911����¬ɪ��������������˲����������ɡ�
�����Ѷȣ�����
2������� �±���Ԫ�����ڱ���һ���֣�
��
���� | I?A | II?A | III?A | IV?A | V?A | VI?A | VII?A
һ
|
��
a
b
?d
e
��
f
g
h
j
|
��1������Ԫ�صĵ������۵���ߵĿ�����______����Ԫ�ط��ţ���д��a���Ȼ���ĵ���ʽ______��e��f��h�γɵļ����ӵİ뾶�ɴ�С˳������Ϊ______�������ӷ��ţ���
��2����һ�������£�j��d���γ�һ�ֻ����������Ϊ����ɫҺ�壬���侧������Ϊ______����������ˮǿ��ˮ�⣬�������ֲ������֮һ�ķ��ӹ���Ϊ�����Σ���һ�����ʾ���Ư���ԣ�д����ط�Ӧ�Ļ�ѧ����ʽ______��
��3������һ��Ԫ�أ���ԭ�ӻ��һ���������ͷų��������ϱ�������Ԫ�������ģ���Ԫ���DZ���______Ԫ�أ����ţ���
��4����g�ĵ���������f���ʣ��γ�����k����g��f��k��Ӳ��������______�����������ƣ���
��5�����Ƶ�117��Ԫ�أ���Ԫ�����ڱ��н�����ǽ����ķ�������Ӧ��һ��______��ѡ����������ǽ�������Ԫ�أ�д��117��Ԫ�����������Ų�ʽ______��
��6�����ö�����Ԫ�أ�д����������ԭ���ӻ�������Ͳ�ͬ��AB3�ͷ��ӵĻ�ѧʽ______��______��
�ο��𰸣���Ԫ�������ڱ���λ�ÿ�֪aΪLiԪ�أ�bΪCԪ�أ�dΪNԪ�أ�eΪFԪ�أ�fΪMgԪ�أ�gΪAlԪ�أ�hΪSԪ�أ�jΪClԪ�أ�
��1��̼���ʴ���ԭ�Ӿ��壬��̼Ԫ�ص����۵������ߣ��Ȼ����������������ӹ��ɣ�����ʽΪ
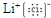
�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС���������Ӱ뾶F-��Mg2+��������������ͬ�����Ӳ�Խ�����Ӱ뾶Խ���������Ӱ뾶S2-��F-���������Ӱ뾶S2-��F-��Mg2+��
�ʴ𰸣�C��
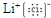
��S2-��F-��Mg2+��
��2��j��d�γɻ�������NCl3��������Ϊ����ɫҺ�壬�е�ϵͣ����ڷ��Ӿ��壮NCl3��ˮǿ��ˮ�⣬�������ֲ������֮һ�ķ��ӹ���Ϊ������ΪNH3����һ�����ʾ���Ư������HClO����Ӧ����ʽΪNCl3+3?H2O�TNH3+3HClO��
�ʴ�Ϊ��NCl3+3?H2O�TNH3+3HClO��
��3��ͬ����������ң��縺������ͬ�������϶��£��縺�Լ�С�����Ե縺�������FԪ�أ�Fԭ�ӻ��һ���������ͷų�������࣬�ʴ�Ϊ��e��
��4���Ͻ��Ӳ�ȸ��ڸ���֣�������þ�Ͻ�Ӳ����ʴ�Ϊ����þ�Ͻ�
��5����������0��Ԫ��Ϊ118�ţ�����117��Ԫ�ش��ڵ������ڵڢ�A�壬���������Ų�ʽΪ7s27p5�������������ܵ��Ӳ��������ڽ���Ԫ�أ�
�ʴ�Ϊ��������7s27p5��
��6��AB3�ͷ��ӿ���Ϊ�����ͣ���NH3��Nԭ�Ӳ�ȡsp3�ӻ���Ҳ������ƽ�������Σ���BF3��Bԭ�Ӳ�ȡsp2�ӻ����ʴ�Ϊ��NH3��BF3��
���������
�����Ѷȣ�һ��
3��ѡ���� ����˵����ȷ����
A.���Ӱ뾶��Ca+��S2-��ԭ�Ӱ뾶��Na��Cl
B.���ϵ��£�±�صķǽ���������������±����������μ���
C.��Ϊ�����ԣ�HClO��ϡH2SO4�����Էǽ����ԣ�Cl��S
D.���ڷ�Ӧ��ʧȥ�ĵ��ӱ����٣����ƵĽ�����С�����Ľ�����
�ο��𰸣�A
���������
�����Ѷȣ�����
4���ƶ��� X��Y��Z��L��M����Ԫ�ص�ԭ��������������X��Y��Z��L����ɵ����ʵĻ���Ԫ�أ�M�ǵؿ��к�����ߵĽ���Ԫ�أ��ش��������⣺
(1)L��Ԫ�ط���Ϊ________��M��Ԫ�����ڱ��е�λ��Ϊ________������Ԫ�ص�ԭ�Ӱ뾶�Ӵ�С��˳����__________________________________(��Ԫ�ط��ű�ʾ)��
(2)Z��X��Ԫ�ذ�ԭ����Ŀ��1��3��2��4���ɷ���A��B��A�ĵ���ʽΪ________��B�ĽṹʽΪ________��
(3)��(Se)������������Ԫ�أ���Lͬһ���壬Seԭ�ӱ�Lԭ�Ӷ��������Ӳ㣬��Se��ԭ������Ϊ________��������������Ӧ��ˮ���ﻯѧʽΪ________������2��5����Ԫ�ص��ʷֱ���H2��Ӧ����1 mol��̬�⻯��ķ�Ӧ�����£���ʾ����1 mol�����ⷴӦ�ȵ���________(����ĸ����)��
a��+99.7 kJ��mol-1 ?b��+29.7 kJ��mol-1? c��-20.6 kJ��mol-1? d��-241.8 kJ��mol-1
(4)��M������������ʯī��������NaHCO3��Һ�����Һ���е�⣬����������R��R���ȷֽ����ɻ�����Q.д����������R�ĵ缫��Ӧʽ��____________________����R����Q�Ļ�ѧ����ʽΪ��________________________��
�ο��𰸣�(1)O���������ڵڢ�A�壻Al��C��N��O��H 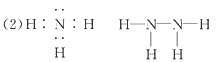
(3)34��H2SeO4��b
(4)Al+3HCO3--3e-===Al(OH)3��+3CO2�� (��Al-3e-===Al3+��Al3++3HCO3-===Al(OH)3��+3CO2��)��
2Al(OH)3 Al2O3+3H2O
Al2O3+3H2O
���������
�����Ѷȣ�һ��
5��ѡ���� ��֪X��YԪ��ͬ���ڣ��ҵ縺��X��Y������˵����������
A.����������ԣ�X��Ӧ������ǿ��Y��Ӧ������
B.��һ������Y��һ��С��X
C.X��Y�γɻ�����ʱ��X�Ը��ۣ�Y������
D.Y����̬�⻯����ȶ���С��X��̬�⻯����ȶ���
�ο��𰸣�A
�������������������ǽ�����Խǿ���縺��Խ��ͬ�����������ҷǽ����������ߣ�����X��ԭ����������Y��ԭ��������A����ȷ������ڶ����ڵ�O��F��û�к�����ģ�B��ȷ�����絪Ԫ�صĵ縺��С����Ԫ�صģ�����һ�����ܴ�����Ԫ�صģ�X�ķǽ�����ǿ��Y�ģ���X��Y�γɻ�����ʱ��X�Ը��ۣ�Y�����ۣ�C��ȷ���ǽ�����Խǿ���⻯����ȶ���Խǿ��D��ȷ����ѡA��
���㣺����縺�Ե��жϺ�Ӧ��
�����������Ǹ߿��еij������ͣ�Ϊ�е��Ѷȵ����⣬������ض�ѧ�������Ŀ��顣������Ҫ��ͨ�����������ų���ɸѡ�õ���ȷ�Ĵ𰸡����ֽ���ķ�����Ҫѧ����ƽʱ��ѵ����ע���ܽ�ͻ��ۣ��ؼ���Ҫ������á�
�����Ѷȣ�����