1、选择题 关于化学键的下列叙述中,正确的是
[? ]
A.离子化合物不可能含共价键
B.共价化合物可能含离子键
C.离子化合物中只含离子键
D.共价化合物中不含离子键
参考答案:D
本题解析:
本题难度:简单
2、选择题 元素X、Y、Z原子序数之和为36,Y、Z在同一周期,X,Z在同一主族,X原子最外层电子数是Y原子最外层电子数的3倍.下列说法正确的是( )
A.同主族元素中X的气态氢化物最稳定
B.Z的最高价氧化物对应的水化物化学式为H3ZO4
C.X与Y可形成共价化合物
D.X与Z所形成的化合物属于酸性氧化物
参考答案:由分析可知X为O元素,Y为Mg元素,Z为S元素.
A、非金属性越强的元素其气态氢化物越稳定,氧族元素中非金属性最强的是O元素,所以氧元素的气态氢化物最稳定,故A正确.
B、Z的最高价氧化物对应的水化物化学式为H2SO4,故B错误.
C、O元素和Mg元素形成的化合物是氧化镁,氧化镁中只含离子键,所以属于离子化合物,故C错误.
D、X和Z形成的化合物SO2、SO3都属于酸性氧化物,故D正确.
故选AD.
本题解析:
本题难度:简单
3、填空题 A、B、C、D、E都是短周期元素,原子序数依次增大;A原子中电子运动的轨道只有一种形状;B、C同周期,A、D同主族.D、B能形成两种离子化合物甲和乙,原子个数比分别为2:1和1:1;E元素原子的最外层电子数是其电子总数的
.根据以上信息回答下列问题:
(1)甲、乙中含有非极性键的物质的电子式是______.
(2)E、C分别形成的氢化物稳定性大小关系是______.(用氢化物的化学式作答)
(3)C和D的离子中,半径较小的是______(填离子符号).画出C和D的离子的结构示意图______,______.
(4)写出B元素基态原子的轨道表示式______.
(5)X是与E同主族的短周期元素,下表列出了X原子间各种共价键的键能:
| 键类型 | X-X | X=X | X≡X
键能(kJ/mol)
159
418
946
|
通过计算说明X2中的______(填“σ键比π键稳定”或“π键比σ键稳定”).
参考答案:A、B、C、D、E都是短周期主族元素,原子序数依次增大,A原子中电子运动的轨道只有一种形状,核外只有1个电子,故A为H元素,A、D同主族,与A的原子序数之差大于2,故D为Na元素,D、B能形成两种离子化合物甲和乙,原子个数比分别为2:1和1:1,故B为氧元素,甲为Na2O,乙为Na2O2,B、C同周期,故C为F元素,E元素原子的最外层电子数是其电子总数的13,E处于第三周期,令最外层电子数为x,则10+x=3x,解得x=5,故E为P元素,则
(1)甲为Na2O,乙为Na2O2,含有非极性键的物质是Na2O2,Na2O2的电子式是
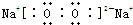
,
故答案为:
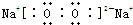
;
(2)非金属性F>P,非金属性越强,氢化物越稳定,故氢化物稳定性为HF>PH3,
故答案为:HF>PH3;
(3)F-与Na+具有相同的电子层结构,核电荷数越大,离子半径越小,故半径较小的是Na+,F-的离子的结构示意图为
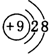
,Na+的离子的结构示意图为
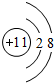
,
?故答案为:Na+,

,
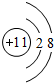
;
(4)B为氧元素,O元素基态原子的轨道表示式
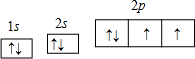
,
故答案为:

;
(5)X是与E同主族的短周期元素,故X为N元素,N-N单键为σ键,键能为159kJ/mol,N=N双键中有1个σ键,1个π键,故N=N双键中π键d键能为418kJ/mol-159kJ/mol=259kJ/mol,N≡N中有1个σ键,2个π键,故N≡N三键中π键的键能为12(946kJ/mol-159kJ/mol)=393.5kJ/mol,键能越大化学键越稳定,故N2中π键比σ键稳定,
故答案为:π键比σ键稳定.
本题解析:
本题难度:一般
4、选择题 下列分子中既不存在s-p σ键,也不存在p-p π键的是
[? ]
A.HCl
B.HF
C.SO2
D.SCl2
参考答案:D
本题解析:
本题难度:简单
5、填空题 过氧化氢(H2O2)的水溶液俗称双氧水,其水溶液可用于制备工业上的漂白剂、特殊环境里燃料燃烧的助燃剂、医疗上的消毒剂、实验室里的制氧剂;过氧化钠(Na2O2)可用于制备工业上的漂白剂、特殊环境里的供氧剂、实验室里的制氧剂。过氧原子团“O2”由2个氧原子共用1对电子组成。 ?
(1)分别写出H2O、Na2O2的电子式:_______、________。 ?
(2)①H2O、H2O2中化学键的不同点是_________________;
②Na2O、Na2O2中化学键的不同点是_________________; ?
③H2O2、Na2O2的化合物类型是(共价化合物、离子化合物)__________________。 ?
(3)分别写出H2O2、Na2O2作供氧剂的化学反应方程式
H2O2:___________________;Na2O2:_______________________。 ?
(4)H2O2与Na2O2相比,化学键更稳定的是(写物质的名称)_______,主要根据是___________________________。?
参考答案:(1)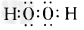 ;
;
(2)①H2O中没有非极性键,H2O2中有非极性键;?②Na2O中没有共价键,Na2O2中有共价键(或非极性键)?;③H2O2是共价化合物,Na2O2是离子化合物?
(3)2H2O2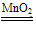 2H2O+O2↑;2Na2O2+2H2O=4NaOH+O2↑或2Na2O2+2CO2= 2Na2CO3+O2?
2H2O+O2↑;2Na2O2+2H2O=4NaOH+O2↑或2Na2O2+2CO2= 2Na2CO3+O2?
(4)过氧化氢;Na2O2在常温下跟水快速反应生成O2,H2O2的水溶液在催化剂作用下才能较快地反应生成O2
本题解析:
本题难度:一般