1、填空题 实验室利用如图装置进行中和热的测定。回答下列问题:
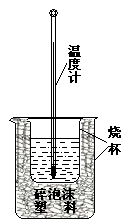
(1)该图中有两处实验用品未画出,它们是?、 ?;
(2)在操作正确的前提下提高中和热测定的准确性的关键是:?。
(3)如果用0.5mol?L-1的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将?(填“偏大”、“偏小”、“不变”)原因是?。
参考答案:⑴环形玻璃搅拌棒、烧杯上方的泡沫塑料盖或硬纸板;
⑵提高装置的保温效果或尽量减少热量损失?⑶偏大?固体NaOH溶于水放热
本题解析:(1)由装置图可以看出:该图中有两处实验用品未画出的是用于混合溶液的环形玻璃搅拌棒;及为了防止热量散失而在烧杯上方盖的泡沫塑料盖或硬纸板。(2)在操作正确的前提下提高中和热测定的准确性的关键是提高装置的保温效果或尽量减少热量损失。(3)由于NaOH溶解在水中会放出热量,所以如果用0.5mol?L-1的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将偏大。
本题难度:一般
2、选择题 下列说法中,正确的是
A.放热反应不需要加热就可以发生
B.化学反应除了生成新物质外,还伴随着能量的变化
C.反应条件为加热的反应都是吸热反应
D.化学反应放热还是吸热,取决于反应条件
参考答案:B
本题解析:A、反应是否加热与反应是放热反应还是吸热反应无关,碳燃烧是放热反应,但需要加热,A不正确;B、化学反应除了生成新物质外,还伴随着能量的变化,这是化学反应的两个基本特征,B正确;C、反应是否加热与反应是放热反应还是吸热反应无关,反应条件为加热的反应不一定都是吸热反应,例如碳燃烧是放热反应,但需要加热,C不正确;D、反应是放热还是吸热与反应条件无关,只与反应物和生成物总能量的相对大小有关系,D不正确,答案选B。
本题难度:一般
3、选择题 CO(g)+H2O(g)  ?H2(g)+CO2(g)?△H<0,在其他条件不变的情况下,下列说明正确的是
?H2(g)+CO2(g)?△H<0,在其他条件不变的情况下,下列说明正确的是
A.加入催化剂,改变了反应的途径,反应放出的热量也随之改变
B.改变压强,平衡不发生移动,反应放出的热量不变
C.升高温度,反应速率加快,反应放出的热量不变
D.若在原电池中进行,反应放出的热量不变
参考答案:B
本题解析:A.加入催化剂,改变了反应的途径,但不改变反应物和产物的能量,故反应放出的热量不改变,故原说法错误;B.改变压强,平衡不发生移动,反应放出的热量不变,正确;C.升高温度,反应速率加快,使上述平衡向吸热方向移动,即逆向移动,反应放出的热量减小,原说法错误;D.若在原电池中进行,将化学能转化为电能了,反应放出的热量大大减少,个原说法不正确。
本题难度:一般
4、选择题 下列说法正确的是:
A.发生分解反应的反应物的总能量一定低于生成物的总能量
B.物质发生化学变化一定伴随着能量变化,且能量形式只表现为热量变化
C.把石墨完全转化为金刚石时,要吸收能量,所以石墨不如金刚石稳定
D.原子结合成分子的过程一定释放出能量
参考答案:D
本题解析:略
本题难度:一般
5、选择题 已知热化学方程式:2H2(g)+O2(g)=2H2O(g) ΔH1=-483.6kJ/mol,则对于热化学方程式:2H2O(l)=2H2(g)+O2(g) ΔH2=b,下列说法正确的是[ ]
A.该反应的ΔH2=+483.6kJ/mol
B.|ΔH2|<|ΔH1|
C.|ΔH2|>|ΔH1|
D.热化学方程式中化学计量数表示分子个数
参考答案:C
本题解析:A 错误,该反应的ΔH2>+483.6kJ/mol ,如果是气态水分解,ΔH2="+483.6kJ/mol" 但该反应是液态水分解,所以吸收的热量要大于483.6kJ,由此可知,B 选项错误,C选项正确,
D 错误,热化学方程式中化学计量数不仅表示分子个数,也表示物质的量。
本题难度:一般