1、选择题 下列实验操作中一定会造成实验值偏小的是(? )
A.将pH试纸用蒸馏水湿润后测某溶液的pH
B.配制500mL 0.10mol/L NaCl溶液,定容时俯视
C.以标准盐酸溶液滴定未知浓度的NaOH溶液时,酸式滴定管未用标准溶液润洗
D.用标准NaOH溶液滴定未知浓度的盐酸溶液,开始时滴定管尖嘴处没有气泡,结束时有气泡
参考答案:D
本题解析:A项用pH试纸测溶液的pH时不能润湿,否则因润润湿导致溶液被稀释使所测pH不准确;B项定容时俯视液面低于刻度线,浓度偏高;C酸式滴定管未用标准溶液润洗,导致标准液浓度偏低,需要的体积偏大,待测液浓度偏高;D项测得标准液体积偏小,待测液浓度偏小。
点评:定量实验中误差分析要依据原理来分析。
本题难度:简单
2、实验题 (18分)某兴趣小组欲从工业食盐中精炼精盐,并配制NaCl溶液,请回答下列问题:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A ??B ?
(2)实验室提纯粗盐的实验操作依次为:
取样、??、沉淀、过滤、??、冷却结晶、烘干。
(3)实验室配制500 mL 0.1mol/L的NaCl溶液,具体操作步骤为:①在天平上称取一定质量的NaCl,把它放在烧杯中,用适量的蒸馏水使其完全溶解;②把制得的溶液小心的注入500 mL的容量瓶中;③继续向容量瓶中滴加蒸馏水至液面距刻度线1~2 cm处时,改用胶头滴管小心滴加,直到溶液的凹液面恰好与刻度线相切为止;④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次的洗涤液都转入容量瓶中,并轻轻摇匀;⑤将容量瓶塞好,充分摇匀。试填写下列空白。
①应该称取的NaCl的质量为________,上述操作的正确顺序是____________;
②本实验用到的仪器除玻璃棒、托盘天平、药匙、烧杯外还需要的有___________________、______________________,
③观察容量瓶中的液面时,若俯视刻度线,会使所配的溶液的浓度________(填“偏高”“偏低”或“无影响”,下同)。没有进行操作④,会________;?
参考答案:(1)Ca(OH)2或CaO;? Na2CO3?(2)溶解;蒸发
(3)①2.9g?①②③④⑤
②500ml容量瓶、胶头滴管③偏高偏低 (每空2分)
本题解析:(1)沉淀剂A来源于石灰窑厂,则A是氢氧化钙或氧化钙。粗盐中含有钙、镁离子等杂质,所以还需要碳酸钠除去钙离子,即B是碳酸钠。
(2)过滤之前需要先溶解,要得到氯化钠晶体,需要蒸发。
(3)①500 mL 0.1mol/L的NaCl中含有0.05mol氯化钠,质量是0.05mol×58.5g/mol=2.925g,所以应该用托盘天平称量2.9g。
②准确配制一定物质的量浓度溶液时需要相应规格的容量瓶,即500ml容量瓶;定容时需要胶头滴管。
③根据c=n/V可知,俯视刻度线,则容量瓶中溶液的体积偏小,浓度偏高;如果没有洗涤,则溶质偏少,浓度偏低。
本题难度:一般
3、实验题 从环己烷可制备1,4-环己二醇的二醋酸酯,下列有关的8步反应(其中所有无机产物都已略去):
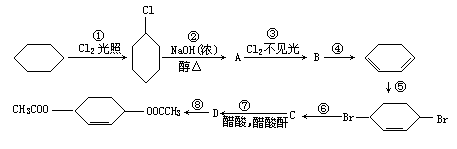
其中有3步属于取代反应,2步属于消去反应,3步属于加成反应。
反应①____和____属于取代反应。
化合物的结构简式是:B____,C_____。
反应④所用试剂和条件是_______。
参考答案:
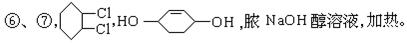
本题解析:环己烷在光照条件下发生卤代反应(取代),生成的卤代烃在NaOH醇溶液作用下发生消去反应生成环己烯(A),在不见光的条件与Cl2发生加成反应(请注意与①反应的区别)生成1,2-二氧环己烷(B),再次在NaOH醇溶液作用下发生消去反应生成1,3-环己二烯,第⑤步反应是与Br2发生加成反应(这个反应类似Br2与1,3-丁二烯发生1,4-加成)。由于反应⑦中加入醋酸与醋酸酐发生酯化反应,所以C应该是醇,

2H2O,⑧有机物与 H2发生加成反应。
本题难度:一般
4、实验题 工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
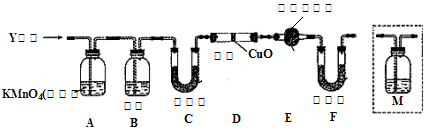
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是?
另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
(2)甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,可选用?(选填序号)。
a.KSCN溶液和氯水?b.K3Fe(CN)6溶液?c.浓氨水?d.酸性KMnO4溶液
参考答案:(10分)
(1)铁钉表面形成致密的氧化物薄膜,阻止铁和硫酸铜反应(或其他合理答案)(2分)
(2)bd(2分)?
(3)检验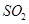 是否除尽(1分)
是否除尽(1分)
(4)C+2H2SO4(浓) CO2+2SO2+2H2O(2分)
CO2+2SO2+2H2O(2分)
(5)c(1分)
(6)D中固体由黑变红和E中固体由白变蓝(2分)
本题解析:(1)该操作使铁钉表面形成致密的氧化物薄膜,阻止铁和硫酸铜反应
(2)X中含有Fe3+,不能用a.KSCN溶液和氯水或c.浓氨水检验,而b.K3Fe(CN)6溶液和d.酸性KMnO4溶液能与Fe2+反应使溶液颜色发生变化,故本题选bd;
点评:对化学实验的考查是历年高考的重点,也是一个难点。解题的关键在于对实验基础知识的掌握,以及对基本实验流程的了解。实验的流程一般遵循“制备装置-除杂装置-性质检验装置-收集装置-尾气处理装置”。
本题难度:一般
5、填空题 二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。ClO2是一种黄绿色的气体,易溶于水。实验室以NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
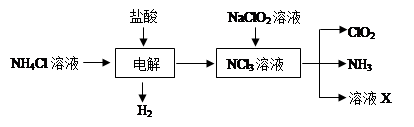
(1)除去ClO2中的NH3可选用的试剂是?;可用于制取NH3的是________(填序号)
A.饱和食盐水
B.碱石灰
C.浓硫酸
D.水 E.NH4HCO3