1、推断题 已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:

(1)D的化学式(分子式)是________,E的化学式(分子式)是___________________。
(2)A和B反应生成C的化学方程式是_________________________________________。
(3)E和F反应生成D、H和G的化学方程式是________________________________。
参考答案:(1)NH3 NH4Cl(2)H2+Cl2 2HCl(3)2NH4Cl+Ca(OH)2
2HCl(3)2NH4Cl+Ca(OH)2 2NH3↑+2H2O+CaCl2
2NH3↑+2H2O+CaCl2
本题解析:E、F两种固体生成CaCl2、气体D和H,可联想氨气的实验室制法:2NH4Cl+Ca(OH)2 2NH3↑+2H2O+CaCl2,E、F可能为NH4Cl或Ca(OH)2,再由C、D气体生成E可知E为NH4Cl,D为NH3、C为HCl,A、B可能是H2或Cl2。
2NH3↑+2H2O+CaCl2,E、F可能为NH4Cl或Ca(OH)2,再由C、D气体生成E可知E为NH4Cl,D为NH3、C为HCl,A、B可能是H2或Cl2。
点评:本题突破口是“E+F→CaCl2+D↑+H”。
本题难度:一般
2、填空题 我国濒临海域的省份,能够充分利用海水制得多种化工产品。如图是以海水、贝壳(主要成分CaCO3)等为原料制取几种化工产品的工艺流程图,其中E是一种化肥,N是一种常见的金属单质。
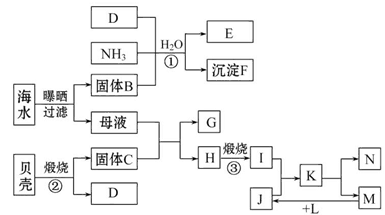
结合上述工艺流程回答下列问题:
(1)物质G和L的化学式分别为___________________和___________________。
(2)上述工艺流程中可以循环使用的物质的化学式为______________________。
(3)反应①的化学方程式为____________;在反应①中必须先通入NH3,而后通入D,其原因是_______________________________________________________。
(4)工业上利用F可制得另一种化工产品,该反应的化学方程式为____________。
(5)由K溶液经如何处理才能制得N?_________________________________________________________。
参考答案:(1)CaCl2?H2?(2)CO2
(3)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
NH3在溶液中的溶解度大,利于吸收CO2,使其转化为NH4HCO3
(4)2NaHCO3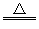 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(5)MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得MgCl2晶体,熔融电解可制取金属镁
本题解析:解答本题应注意以下两点:
(1)联系与海水综合利用相关的工业生产分析工艺流程图。
(2)明确工艺流程图中各字母对应的物质。
题中的工艺流程图由海水晒盐、海水提镁和工业制纯碱三部分组成。分析工艺流程图中的转化关系可得,B、C、D、E、F、G、H、I、J、K、L、M、N分别是NaCl、CaO、CO2、NH4Cl、NaHCO3、CaCl2、Mg(OH)2、MgO、HCl、MgCl2、H2、Cl2、Mg。
(1)物质G和L的化学式分别为CaCl2、H2。
(2)在用贝壳制生石灰时同时生成CO2,在将NaHCO3加热分解制纯碱时也生成CO2,CO2可循环利用。
(3)反应①是用NaCl、NH3、CO2和H2O反应制取NaHCO3和NH4Cl的反应,化学方程式为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。NH3在水溶液中的溶解度大,利于吸收较多量的CO2使其转化为NH4HCO3。
(4)工业上用NaHCO3受热分解可制得纯碱,化学方程式为:2NaHCO3 Na2CO3+
Na2CO3+
CO2↑+H2O。
(5)MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,再电解熔融MgCl2可制得金属镁。
本题难度:一般
3、简答题 在下列中学化学中常见物质的转化关系图中,已知常温下A为淡黄色固体化合物、B为金属单质,D、E、M是常见气体单质,其中I为红褐色固体,M为黄绿色,N是胃酸的主要成分,工业上用E和M来制取N,试推断:
(1)写出下列化学式?A______?I______
(2)G转化为I的现象为______
(3)F+M→H离子方程式为______
(4)A+X→C+D的化学方程式为______.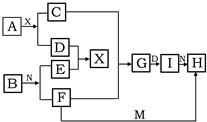
参考答案:已知常温下A为淡黄色固体化合物判断为Na2O2;B为金属单质,D、E、M是常见气体单质,其中I为红褐色固体判断为Fe(OH)3,M为黄绿色为Cl2,N是胃酸的主要成分推断为HCl,H为FeCl3;工业上用E和M来制取N,说明E为H2,依据转化关系中的反应可知,C为NaOH,D为O2,X为H2O,由推断出I判断,G为Fe(OH)2,F为FeCl2,确定B为Fe;
(1)依据分析判断A为:Na2O2 ;?I的化学式为:Fe(OH)3;故答案为:Na2O2 ;Fe(OH)3;
(2)G(Fe(OH)2)转化为I(Fe(OH)3)的现象是:白色沉淀迅速变为灰绿色,最后变为红褐色;故答案为:白色沉淀迅速变为灰绿色,最后变为红褐色;
(3)F(FeCl2)+M(Cl2)→H(FeCl3),反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-;故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(4)A(Na2O2)+X(H2O)→C(NaOH)+D(O2),反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑;
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
本题解析:
本题难度:一般
4、填空题 有A、B、C三种常见的金属单质,A在空气中燃烧生成淡黄色固体;B也能在空气中剧烈燃烧,发出耀眼的白光;C在一定条件下与水蒸气反应生成H2和一种黑色固体。根据以上信息回答下列问题:
(1)写出化学式A??B??C??
(2)写化学方程式①A在空气中燃烧?
②C与水蒸气反应?
③A与水反应?
参考答案:(1)A? Na??B? Mg??C? Fe??
(2)①? ?
?
②?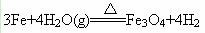 ?
?
③? 2Na+2H2O===2NaOH+H2↑?
本题解析:略
本题难度:简单
5、填空题 (6分)有X、Y、Z、W四种短周期元素,原子序数依次增大,其核电荷总数为36。Y元素原子最外层电子数占其核外电子总数的3/4,W元素原子最外层电子比同周期Z元素多5个电子,W和Y属于同一主族。
(1)写出元素符号:X______Y_________Z________W___________.?
(2)Z、W两元素的最高价氧化物对应水化物反应的离子方程式是__________
参考答案:(6分)(1)写出元素符号:X__H__Y__O___Z__Na___W__S__.?
(2)离子方程式是_略
本题解析:略
本题难度:一般