1、填空题 (5分)利用下述反应 2FeCl3+Cu=2FeCl2+CuCl2设计一个原电池装置;试回答:(1)(3分)该原电池的正极材料是 ,负极材料是 , 电解质溶液是 。
(2)该原电池的负极反应式为 ,正极反应式为
。
2、填空题 (1)将一块纯净的锌片插入盛有稀硫酸的烧杯里,可观察到锌片逐渐溶解,并有气体产生,再平行地插入一块铜片,可观察到铜片上______(填“有”或“没有”)气泡产生.用导线将锌片和铜片连接起来(如图a所示),可观察到铜片上______?(填“有”或“没有”)气泡产生.
(2)用导线连接灵敏电流计的两端后,再与溶液中的锌片和铜片相连接(如图b所示),观察到灵敏电流计的指针发生偏转,说明导线中有电流通过.从上述现象可以归纳出构成原电池的某些条件是:______,电极反应式是:锌片______;铜片______.
(3)可见,图b是一个将______能转化为______能的装置,被称为原电池.我们也可以用家庭常见的一些仪器和物品,自制一个原电池,请你尝试涉及实验,并将你所设计的原电池简图画在右面的方框内:
所需物品及仪器:______.
实验操作步骤及现象:______.

3、选择题 有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(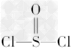 )中而形成的,电池总反应方程式为:8Li+3SOCl2===6LiCl+Li2SO3+2S,下列叙述中正确的是
)中而形成的,电池总反应方程式为:8Li+3SOCl2===6LiCl+Li2SO3+2S,下列叙述中正确的是
[? ]
A.电解质溶液中混入水,对电池反应无影响
B.金属锂作电池的正极,石墨作电池的负极
C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4∶1
4、选择题 下列有关电池的说法错误的是?
A.手机上用的锂离子电池属于二次电池
B.铅蓄电池中负极为铅,电解质是硫酸
C.氢氧燃料电池正极输入氢气,负极输入空气
D.锌锰干电池即使不用,长久放置也会失效
5、填空题 (14分)聚合氯化铝是一种新型净水剂,其中铝的总浓度(用AlT表示)包括三类‘“主要为Al3+的单体形态铝总浓度(用Ala表示);主要为[AlO4Al12(OH)24(H2O)12]7+的中等聚合形态铝总浓度(用Alb表示)和Al(OH)3胶体形态铝总浓度(用A1c表示)。
(1)一定条件下,向1.0 mol/LAlCl3溶液中加入0.6 mol/L的NaOH溶液,可制得Alb含量约为86%的聚合氯化铝溶液。写出生成[AlO4Al12(OH)24(H2O)12]7+的离子方程式:_____________________。
(2)用膜蒸馏(简称MD)浓缩技术将聚合氯化铝溶液进行浓缩,实验过程中不同浓度聚合氯化铝中铝形态分布(百分数)如下表:
AlT/(mol・L-1)
| Ala/%
| Alb/%
| A1c/%
|
0.208
| 1.4
| 86.6
| 12.0
|
0.489
| 2.3
| 86.2
| 11.5
|
0.884
| 2.3
| 88.1
| 9.6
|
1.613
| 3.1
| 87.0
| 9.9
|
2.520
| 4.5
| 88.2
| 7.3
|
①在一定温度下,AlT越大,pH (填“越大”、“越小”或“不变”)。
②如将AlT =" 2.520" mol・L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式: 。
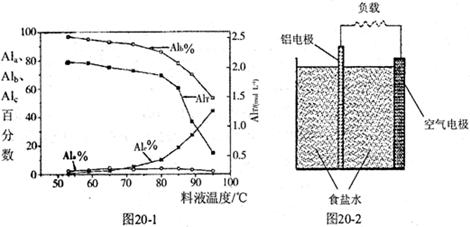
③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图20―1。当T>80℃时,AlT显著下降的原因是 。
(3)真空碳热还原一氧化法可实现由铝土矿制备金属铝,相关反应的热化学方程式如下:
①Al2O3(s)+AlCl3(g)+3C(s) = 3AlCl(g)+3CO(g) △H1 =" a" kJ・mol-1
②3AlCl(g) =" 2Al(l)+" AlCl3(g) △H2 =" b" kJ・mol-1
则反应Al2O3(s)+ 3C(s) =" 2Al(l)+" +3CO(g) △H = kJ・mol-1(用含a、b的代数式表示)。反应①常压下在1900℃的高温下才能进行,说明△H 0(填“>”“=”或“<”)。
(4)一种铝空气电池结构如图20-2所示,写出该电池正极的电极反应式 。