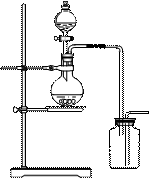
1、实验题 (12分)I.下图是某学生设计的制取和收集某些气体的实验装置(可加热)。
(1)该装置在加入反应物前,应首先进行的实验操作是?。
(2)下列气体的制取中,若用排空气法收集,可使用该装置制备和收集的是(选填编号,下同)__________若用排水法收集(集气瓶中充满水),可使用该装置制备和收集的是? ___________。
①用Zn与稀盐酸反应制H2?
②用CaCO3与稀盐酸反应制CO2?
③用固体NaOH和浓氨水制NH3?
④用Cu与稀HNO3反应制NO
⑤用MnO2与双氧水反应制O2
⑥浓硫酸与铜片反应制SO2
⑦用MnO2与浓盐酸反应制Cl2
II. 某校化学研究性学习小组对浓硫酸与金属锌的反应进行探究。首先按图组装好实验装置,然后取一定量的浓硫酸与足量Zn充分反应,微热试管A,实验过程中先观察到C、D中均有气泡产生,D中开始出现浑浊,后浑浊消失,随后气泡量逐渐减少,品红溶液褪色,反应较长时间后,C、D中的气泡量又 会明显增加。
会明显增加。
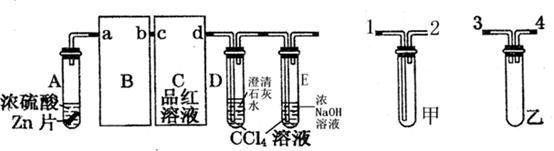
试回答:
(1)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接?、?接b,c接?、?接d;
(2)D、E试管中CCl4溶液的作用是防止溶液倒吸,该实验中起到同样作用的装置是____________;
(3)能证明浓硫酸具有强氧化性的实验现象为?;
(4)反应较长时间后气泡量又会明显增加的原因是?;
(5)D中浑浊消失的离子方程式为?。
参考答案:I、(1)检查装置气密性 (1分) (2)①③;①④⑤;(各2分)
II、(1)3或4? 4或3(1分)? 1? 2(1分)
(2)乙(填B也得分)(1分)
(3)C中品红溶液褪色(1分)?
(4)浓H2SO4变成 稀H2SO4,与Zn反应放出H2(1分)
稀H2SO4,与Zn反应放出H2(1分)
(5)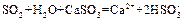 (2分)
(2分)
本题解析:略
本题难度:一般
2、实验题 氮及其化合物在生产、生活中有重要的作用。
(1)NH3是制碱工业中不可缺少的重要物质。继侯德榜“联合制碱法”后,上世纪50年代某些化工专家开始研究有机胺制碱法,其工艺流程如下:
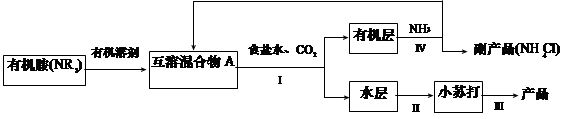
已知:NR3 + CO2 + NaCl + H2O = NaHCO3 + NR3・HCl
NR3 + HCl = NR3・HCl,且NR3・HCl 易溶于有机溶剂。
①操作Ⅰ名称为?;
②某实验小组同学查阅资料知,有机溶剂和有机胺沸点差别较大,现欲将A中各成分进行分离,请写出除了导管、酒精灯、牛角管、锥形瓶外,该分离操作所需的玻璃仪器名称 ?;
(2)N2在化工生产、农业、医疗、航天航空等领域用途广泛。现提供以下装置(连接仪器略去):
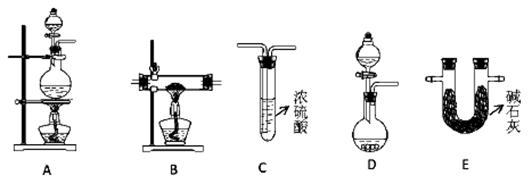
①某化学兴趣小组甲同学欲用加热NaNO2 和NH4Cl的浓溶液制得N2,应该选择的发生装置是?,检验该发生装置气密性的操作为 ?;
②在加热条件下,用NH3 还原CuO可制得N2,同时获得铜粉,此反应的化学方应方程式是?。乙同学用此法制得干燥、纯净的N2,且需要的NH3 以生石灰和浓氨水作原料。按气流从左到右,整套装置的连接顺序是?(填写字母序号);最后一个装置中试剂的作用是??;
参考答案:(1)①分液(2分)
②蒸馏烧瓶、温度计、冷凝管(2分,答对2种得1分,全答对得2分)
(2)①A (2分);关闭分液漏斗下端活塞并将导管连接长导管后置于水中(1分),用酒精灯微热圆底烧瓶,若导管口有气泡冒出,撤掉酒精灯后导管内有一段水柱,则装置气密性好(1分);反之,则装置气密性不好。
②3CuO+ 2NH3 N2+ 3Cu + 3H2O(2分);DEBC(2分);干燥N2(1分)并除去其中的NH3(1分)
N2+ 3Cu + 3H2O(2分);DEBC(2分);干燥N2(1分)并除去其中的NH3(1分)
本题解析:(1)①分离互补相溶液体的方法是分液,所以操作Ⅰ名称为分液。
②有机溶剂和有机胺沸点差别较大,可用蒸馏分离,根据蒸馏的仪器:带铁圈的铁架台,酒精灯,石棉网,蒸馏烧瓶,温度计,冷凝管,牛角管,锥形瓶,因此还缺少蒸馏烧瓶、温度计、冷凝管。
(2)①根据已知信息可知,反应物是亚硝酸钠(NaNO2)和氯化铵的浓溶液混合加热制备氮气,所以需要圆底烧瓶作反应容器,同时还需要加热,因此A装置适合;检验装置气密性的方法一般是利用压强差来进行,所以正确操作是安装好仪器后,关闭分液漏斗下端活塞并将导管连接长导管后置于水中,用酒精灯微热圆底烧瓶,若导管口有气泡冒出。撤掉酒精灯后导管内有一段水柱,则装置气密性好;反之,则装置气密性不好。
②根据原子守恒可知,NH3与CuO反应生成N2、铜和水,所以反应的化学方程式为3CuO+ 2NH3 N2+ 3Cu + 3H2O;需要的NH3 以生石灰和浓氨水作原料,因此需要用D用来制取氨气,氨气是碱性气体,不能用浓硫酸干燥,应该用E装置(碱石灰)干燥氨气。在B中反应后,剩余的氨气可用C装置来除去,同时C装置中的浓硫酸还能干燥氮气。所以按气流从左到右,整套装置的连接顺序是DEBC。
N2+ 3Cu + 3H2O;需要的NH3 以生石灰和浓氨水作原料,因此需要用D用来制取氨气,氨气是碱性气体,不能用浓硫酸干燥,应该用E装置(碱石灰)干燥氨气。在B中反应后,剩余的氨气可用C装置来除去,同时C装置中的浓硫酸还能干燥氮气。所以按气流从左到右,整套装置的连接顺序是DEBC。
本题难度:一般
3、填空题 (10分)某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,有人设计如下实验:
(1)取样品a g。
(2)将样品溶于足量稀盐酸中,过滤,滤液中主要含有的金属阳离子为________;滤渣中含有的物质为____________;
(3)往滤液中加入过量NaOH溶液,过滤,写出该步操作中与铝的化合物有关的离子方程式_____________________________。
(4)在第(3)步的滤液中通入足量CO2,过滤,将沉淀用蒸馏水洗涤数次后,烘干并灼烧至重量不再减少为止,冷却后称量,质量为b g。写出足量CO2通入滤液中所涉及的化学方程式________________。
(5)计算:该样品中铝的质量分数的表达式为___________________________。
参考答案:(10分) 1.(2)Mg2+、Al3+ (2分)? Cu、Si (2分)
(3) Al3++3OH-===Al(OH)3↓,Al(OH)3+OH-===AlO2-+2H2O
或Al3++4OH-=AlO2-+2H2O?(2分)
(4)NaAlO2+CO2+2H2O===NaHCO3+Al(OH)3↓?(2分)(5) 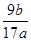 ×100%?(2分)
×100%?(2分)
本题解析:(2)单质铜和硅与盐酸不反应,所以将样品溶于足量稀盐酸中,过滤,滤液中主要含有的金属阳离子为Mg2+、Al3+,滤渣中含有的物质为Cu、Si。
(3)由于氢氧化铝是两性氢氧化物,所以往滤液中加入过量NaOH溶液,生成氢氧化镁白色沉淀,而铝离子先生成氢氧化铝白色沉淀,然后又溶解,反应的离子方程式分别是Al3++3OH-===Al(OH)3↓,Al(OH)3+OH-===AlO2-+2H2O或Al3++4OH-=AlO2-+2H2O。
(4)偏铝酸钠能和CO2反应生成氢氧化铝白色沉淀,由于CO2过量,所以反应的化学方程式是NaAlO2+CO2+2H2O===NaHCO3+Al(OH)3↓。
(5)最终生成的是氧化铝,质量是bg,则根据原子守恒可知,该样品中铝的质量分数的表达式为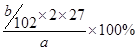 =
=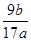 ×100%。
×100%。
点评:该题是中等难度的试题,试题贴近高考,难易适中,注重能力的培养和解题方法的训练,注重解题的灵活性。有利于培养学生的逻辑推理能力和发散思维能力,提高学生分析问题、解决问题的能力。有助于提高学生的应试能力和灵活应变能力。
本题难度:一般
4、选择题 用如图所示的装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是
选项
| 气体
| a
| b
| c
|
A
| CO2
| 稀盐酸
| 石灰石
| 浓硫酸
|
B
| SO2
| 浓硫酸
| 铁片
| 浓硫酸
|
C
| NH3
| 浓氨水
| 生石灰
| 碱石灰
|
D
| Cl2
| 浓盐酸
| MnO2粉末
| 浓硫酸
|
?
参考答案:A
本题解析:B、常温下,铁遇浓硫酸钝化,得不到SO2,错误;C、氨气应用向下排空气法收集,错误D、MnO2与浓盐酸需加热才能反应,错误。
本题难度:一般
5、实验题 某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)
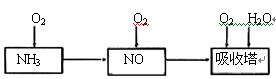

(1)工业上用氨气制取NO的化学方程式是?。
(2)连接好装置后,首先进行的操作是?。
(3)通入a气体的目的是?.
(4)盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中发生反应的化学方程式是
2NO2+Na2CO3=====NaNO2+?+?
(5)已知:温度低于21.15°C时,NO2几乎全部转变为N2O2。工业上可用N2O4与水反应来提高硝酸产率。N2O4与a气体在冷水中生成硝酸的化学方程式是?。
 ?(6)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.500mol/L,c(N2O4)=0.125mol/L。则2NO2(g)? N2O4(g)的平衡常数K=?。若NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为?。
?(6)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.500mol/L,c(N2O4)=0.125mol/L。则2NO2(g)? N2O4(g)的平衡常数K=?。若NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为?。
参考答案:
(1)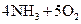
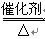 4NO+6H2O
4NO+6H2O
(2)检验装置的气密性
(3)提高NO2的转化率(或2NO+O2=2NO2)(合理均给分)
(4)NaNO3? CO2
(5)2N2O4+O2+2H2O=4HNO3
(6)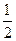 ? 50%
? 50%
本题解析:略
本题难度:一般