1������� ��11�֣�����������װ�ü��Լ���װһ��װ�á��������ǣ���Ũ�����MnO2����ȡ���������Cl2�����ռ���������������Cl2�ͳ�ʪ��Cl2����Ư���ԡ��Իش�
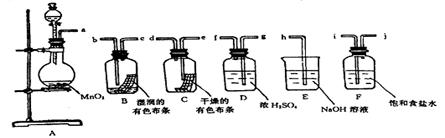
��1�������������������װ������������������ӿڱ�ţ���
? a?��?��?��?��?��?��?��?��?��? h?��
װ���д���ʲô����?��
��2����ƿ�з�����Ӧ�Ļ�ѧ��Ӧ����ʽ��?��
��3��Dװ�õ�������?��Fװ�õ�������?��
��4��Cƿ�е�������?��������ʵ˵����Ư�����õ�������?��
��5��E�з�Ӧ�����ӷ���ʽ��?��
�ο��𰸣���1��ijg f e d b c��2�֣�? Aװ��ȱ�پƾ��ƣ�1�֣�
��2��MnO2 + 4HCl 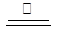 ?MnCl2 + 2H2O + Cl2����2�֣�
?MnCl2 + 2H2O + Cl2����2�֣�
��3������������1�֣�?��ȥHCl���壨1�֣�
��4����ɫ��������ɫ��1�֣�?�����ᣨ1�֣�
��5��Cl2+2OH��=ClO��+Cl��+H2O��2�֣�
�����������1������ʵ��װ�á�����װ�á����ʼ���װ�á�β������װ��������Ϊ���������壬�ʳ����ܽ����̵��ܳ�������ʳ��ˮ����ˮ�֣�Ũ���������ˮ�����Ƚӱ���ʳ��ˮ���ٽ�Ũ���ᡣ��2������ʵ����ʵ��д����3��Ũ���������ˮ�ԣ��Ҳ���������Ӧ������Ũ�����������������ʳ��ˮ���Խ����������ܽ�ȣ�����������ȥ������Ȼ������塣��4��Cƿ�еIJ�������ɫ��˵����Ư�����õIJ�����������������ˮ��Ӧ���ɴ����ᣬʪ�����ɫ������ɫ��˵����Ư�����õ��Ǵ����ᡣ��5������ʹ�ж����壬����ֱ����������У��������������ա�
�����������������ۺ�֪ʶ�����������Ӧע��һ�����ݣ���Ũ�����ܺ�MnO2��Ӧ��ϡ������ԣ��ڴ����������ᣬ����ǿ������
�����Ѷȣ�һ��
2��ѡ���� ����װ�ò��ܴﵽ��Ӧʵ��Ŀ�ĵ��ǣ�?��?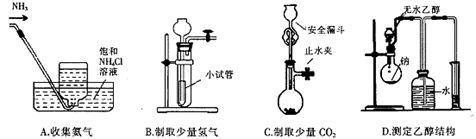
�ο��𰸣�A
���������
������������ˮ����������ˮ���ռ��������ܶ�С�ڿ�����Ӧ���������ſ������ռ���������A�𰸴���ѡA��
�����Ѷȣ���
3��ʵ���� �Է���мΪԭ���Ʊ�FeCl3��Һ������ӡˢ��·ͭ�帯ʴ����������ҺB���е�����ʵ���������£�

(1)�Լ�aӦѡ��?(��д����)��
(2)����I�õ�����Ҫ����������©����?(��д��������)��
(3)д�����������Ҫ��Ӧ�Ļ�ѧ����ʽ��?��
(4)ʵ������ȡ����E�����ӷ���ʽ��?����������E���и�������գ���ѡ������װ���е�?(��д���)��
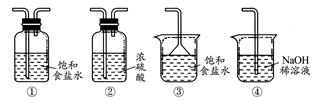
(5)����û�ѧ������������E��?��
�ο��𰸣�(1)ϡ����
(2)�ձ���������
(3)2FeCl3��Cu=2FeCl2��CuCl2
(4) MnO2��4H����2Cl�� Mn2����Cl2����2H2O���ڢ�
Mn2����Cl2����2H2O���ڢ�
(5)��ʪ���KI?������ֽ��������ƿ�ڣ���ֽ������֤��������ΪCl2��
������������������е����ʼ��仯ѧ��Ӧ������м�м����ȼ�Һ��Ϊ�˳�ȥ��м��������ۣ���Fe��Ӧ����Fe2�����Լ�ֻ��ѡ��HCl��������A��Cl2����������FeCl3��������H2SO4��HNO3�������ᣬ������SO42-��NO3-�����ʡ��������õIJ��������У�©�����ձ�����������2FeCl3��Cu=2FeCl2��CuCl2����B�к���FeCl2��CuCl2��FeCl3�����ʣ�������ʱ�����������ӷŵ�˳��������Cu����������Cl2����������������Fe3��>Cu2������Fe3��һ���ŵ��Fe2�������Cu����������Cl2��ʵ�����Ʒ�ΪMnO2��Ũ���ᷴӦ����Cl2�л���HCl��H2O�����ʣ�����Cl2�âڣ�����Cl2�âܣ�Cl2�ļ��鷽������ʪ��ĵ���?KI��ֽ��
�����Ѷȣ�һ��
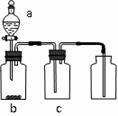
4��ѡ���� ����ͼװ����ȡ���ᴿ���ռ����е��������壨a��b��c��ʾ��Ӧ�����м�����Լ��������п��е���
?
| ����
| a
| b
| c
| 
|
A
| NH3
| Ũ��ˮ
| ������
| Ũ����
|
B
| SO2
| Ũ����
| Cu
| ���Ը��������Һ
|
C
| O2
| ˫��ˮ
| ��������
| ��ʯ��
|
D
| CO2
| ϡ����
| CaCO3
| ����NaHCO3��Һ
|
?
�ο��𰸣�D
���������A���������ܶ�С�ڿ������ܶȣ�����Ӧ�������ſ����������ռ����Ҳ�����Ũ������ﰱ������A����ȷ��B��Ũ�����ͭ��Ӧ��Ҫ���Ȳ��ܲ����������������Ը��������Һ������SO2����B����C��ϴ��ƿ��Ӧ��ʢ��Һ������Ũ���ᣬC����ȷ��D����Ӧװ��Ϊ��Һ��ϲ�������װ�ã�ʵ������̼��ƺ�ϡ���ᷴӦ��ȡ������̼���ҿ����ñ���̼��������Һ��ȥ�Ȼ��⣬��D��ȷ����ѡD��
�����Ѷȣ�һ��
5��ʵ���� [ʵ�黯ѧ]
��������������ҽҩ���й���ϵȹ�ҵ��Ӧ�ù㷺���Զ������ױ���Ϊԭ����ȡ������������(��ɫ�ᾧ���۵�242 �棬�е�Լ359 �棬����ˮ����������)�ķ�Ӧԭ��Ϊ��
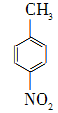 ��Na2Cr2O7��4H2SO4�D��
��Na2Cr2O7��4H2SO4�D��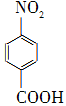 ��Na2SO4��Cr2(SO4)3��5H2O
��Na2SO4��Cr2(SO4)3��5H2O
ijС���Զ������ױ�������Ϊԭ����ȡ�������������ʵ��װ������ͼ��ʾ(���Ⱥ������̶�װ�þ�����ȥ)��ʵ�鲽�����£�

����1����250 mL������ƿ�����μ��������Ķ������ױ����ظ����Ʒ�ĩ��ˮ������ֻ�ϡ��ڽ����£��õ�Һ©����������Ũ�������0��5 h����ӦҺ�ʺ�ɫ��
����2������Ӧ�������ȴ��������ˮ��ֻ�ϣ����˲���50 mLˮ������ϴ�ӡ���ϴ�Ӻ�Ĺ������ʢ������5%������Һ�У�ˮԡ����10 min����ȴ����ˡ�
����3�������˺�Ĺ�����������5%NaOH��Һ�У�50 �����Ⱥ���ˣ�����Һ�м�����������̿����к���ȳ��ˡ����õ�����Һ�������뵽ʢ������15%������Һ���ձ��У�������ɫ���������ˣ���ˮϴ�ӣ�����ôֲ�Ʒ����
��1�� �ڲ���1�С����衱���õ綯��������ɵģ����������ĺô���________��________��
��2�� ��������ƿ�У�����Ũ����ļ��룬��Ӧ�¶�Ѹ��������Ϊʹ��Ӧ�¶Ȳ��¹��ߣ���Ҫʱ�ɲ�ȡ�Ĵ�ʩ��________��
��3�� �ڲ���2�У��������ù������Ҫ�ɷ���________������װ������������������ѹϵͳ�⣬����________��________(����������)��
��4�� ����3��NaOH��Һ���д�����������Ҫ��____��
��NaOH��Һ��������50 �����Ⱥ���˵�ԭ����____��
��5�� �ƵõĴֲ�Ʒ��Ҫ��һ������(����)�����ݶ�������������й����ʿ�֪��������о���(����)�������Ҵ���Һ��ɣ�Ҳ���Բ���________����ɡ�
�ο��𰸣�
��1�� ʹ��Ӧ��Ѹ�ٻ�Ͼ��ȣ����Ա��ⷴӦ��ֲ����ȡ���Ũ�����¸���Ӧ�������ܹ����̷�Ӧʱ�����߲���(�δ����㡣���������𰸾���)(2��)
��2�� �ñ�ˮ��ȴ(���������𰸾���)(1��)
��3�� ������������(1��)������ƿ(1��)������©��(1��)
��4�� (��һ��)��ȥ���ʸ���[����Cr(OH)3����](���������𰸾���)(2��)
���¶ȹ��ͣ��������������ƻ����������˳�(2��)
��5�� ����(���������𰸾���)(2��)
�����������1���������ʹ��Ӧ��Ѹ�ٻ�Ͼ��ȣ����Ա��ⷴӦ��ֲ����ȡ���Ũ�����¸���Ӧ�������ܹ����̷�Ӧʱ�����߲��ʣ���2��ʹ��Ӧ��ϵ���¶��½����Բ��ñ�ˮ��ȴ�ķ�ʽ����3����Ӧ�����в���1�Ƿ�Ӧ�����������������ƣ�����2����������������ữΪ���������������3�dz�ȥ�������ʣ���4���ò��dz�ȥ��Ԫ���γɵ������������¶ȵͶ������������ƻ����������˳���ɲ�Ʒ��ʧ����5�������������������������Բ������������ӡ�
�����Ѷȣ�һ��