1、选择题 发生原电池的反应通常是放热反应,在理论上可设计成原电池的是
A.C(s)+H2O(g)=CO(g)+ H2(g);△H>0
B.Ba(OH)2.8H2O(s)+2NH4Cl(s)=BaCl2(aq)+2NH3.H2O(1) +8H2O(1);△H>0
C.CaC2(s)+2H2O(1)→Ca(OH)2(s)+C2H2(g);△H<0
D.CH4(g)+2O2(g)→CO2(g) +2H2O(1);△H<0
参考答案:D
本题解析:发生原电池的反应通常是放热反应而且是氧化还原反应,A是吸热反应,B、C是非氧化还原反应
本题难度:一般
2、填空题 如图甲、乙是电化学实验装置。
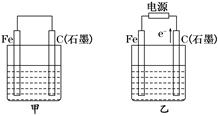
(1)若甲、乙两烧杯中均盛有NaCl溶液.
①甲中石墨棒上的电极反应式为____________________________________________。
②乙中总反应的离子方程式为______________________________________________。
③将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2.若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为__________________________________________________________________。
(2)若甲、乙两烧杯中均盛有CuSO4溶液.
①甲中铁棒上的电极反应式为____________________________________________。
②如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入________(填写物质的化学式)________ g。
参考答案:(1)①2H2O+O2+4e-===4OH-
②2Cl-+2H2O  ?H2↑+Cl2↑+2OH-
?H2↑+Cl2↑+2OH-
③5Cl2+I2+6H2O === 10HCl+2HIO3
(2)①Fe-2e- === Fe2+
②CuO(或CuCO3) 0.8(或1.24)
本题解析:(1)若两烧杯中均盛有NaCl溶液,则:①甲装置为原电池,石墨棒作正极,O2放电,电极反应为:O2+2H2O+4e- === 4OH-.②乙装置为电解池,石墨棒上发生氧化反应,Fe电极不参与反应,其实质与用惰性电极电解食盐水相同,离子方程式为:2Cl-+2H2O  ?Cl2↑+H2↑+2OH-.③Cl2和I2的物质的量之比为5∶1,生成HCl和HIO3.(2)若两烧杯中均盛有CuSO4溶液,则:①甲装置为原电池,铁作负极,电极反应为:Fe-2e- === Fe2+.②乙装置为电解池,电解反应为:2CuSO4+2H2O
?Cl2↑+H2↑+2OH-.③Cl2和I2的物质的量之比为5∶1,生成HCl和HIO3.(2)若两烧杯中均盛有CuSO4溶液,则:①甲装置为原电池,铁作负极,电极反应为:Fe-2e- === Fe2+.②乙装置为电解池,电解反应为:2CuSO4+2H2O  ?2Cu+2H2SO4+O2↑,根据电解方程式,从电解质溶液中析出Cu,放出O2,因此只需加入CuO(或CuCO3)即可恢复到电解前的状态.由电解反应式可知,2H+~CuO~CuCO3,电解后n(H+)=0.1×0.2=0.02(mol),
?2Cu+2H2SO4+O2↑,根据电解方程式,从电解质溶液中析出Cu,放出O2,因此只需加入CuO(或CuCO3)即可恢复到电解前的状态.由电解反应式可知,2H+~CuO~CuCO3,电解后n(H+)=0.1×0.2=0.02(mol),
故m(CuO)=0.02×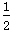 ×80=0.8(g),m(CuCO3)=0.02×
×80=0.8(g),m(CuCO3)=0.02×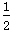 ×124=1.24(g).
×124=1.24(g).
点评:本题考查原电池的设计及原电池的工作原理,题目难度中,注意从氧化还原反应的角度确定原电池的电极材料及电解质溶液。
本题难度:一般
3、选择题 下列叙述正确的是?
[? ]
A.反应NH3(g)+HCl(g)=NH4Cl(s)?△H<0,在任何条件下均能自发进行
B.铅蓄电池在放电过程中,负极质量减小,正极质量增加
C.温度一定时,水的离子积常数Kw不随外加酸(碱)浓度的改变而改变
D.由于Ksp(BaSO4)小于Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀
参考答案:C
本题解析:
本题难度:一般
4、选择题 如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是: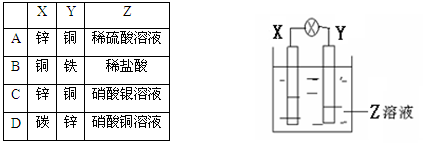
参考答案:D
本题解析:活泼金属做负极,依题意可知X为正极Y为负极,AC错误。正极没有气泡产生,D正确。
本题难度:一般
5、选择题 化学与科学、技术、社会和环境密切相关。下列有关说法中错误的是
A.对废旧电池进行回收处理,主要是为了环境保护和变废为宝
B.用电解水的方法制取大量H2,可以缓解能源不足的问题
C.大力开发和应用氢能源有利于实现“低碳经济”
D.工业上,不能采用电解MgCl2溶液的方法制取金属镁
参考答案:B
本题解析:A、废旧电池中含有重金属,因此对废旧电池进行回收处理,主要是为了环境保护和变废为宝,A正确;B、电解水需要消耗大量的电能,不利于节能,B不正确;C、氢能是新能源,因此大力开发和应用氢能源有利于实现“低碳经济”,C正确;D、镁是活泼的金属,工业上,不能采用电解MgCl2溶液的方法制取金属镁,而是电解熔融的氯化镁,D正确,答案选B。
本题难度:简单