1、填空题 现有下列七种物质:
①铝?②蔗糖?③CO2?④H2SO4?⑤Ba(OH)2?⑥红褐色的氢氧化铁胶体?⑦HCl
(1)上述物质中属于电解质的有?。(填序号)
(2)向⑥的溶液中逐渐滴加⑦的溶液,看到的现象是?。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为?。
参考答案:(1)④、⑤、⑦
(2)开始产生红褐色沉淀,后来沉淀溶解消失
(3)Ba(OH)2+2HCl=BaCl2+2H2O
本题解析:(1)①铝是单质既不是电解质也不是非电解质; ②蔗糖不导电;③CO2溶于水生成的H2CO3导电,本身不导电;④H2SO4导电是电解质。⑤Ba(OH)2导电,是电解质;⑥红褐色的氢氧化铁胶体,不是电解质;⑦HCl是强电解质。(2)向⑥的溶液中逐渐滴加⑦的溶液,看到的现象是开始产生红褐色沉淀,后来沉淀溶解消失。(3)Ba(OH)2+2HCl=BaCl2+2H2O
本题难度:一般
2、填空题 如图:某溶液中含有Ba2+、Cu2+、Ag+,用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。(写出最佳答案)

(1)沉淀的化学式是:沉淀1_________,沉淀2_________,沉淀3_________。
(2)写出混合液+A的离子方程式:___________________________
写出溶液+B的离子方程式:___________________________
参考答案:(1)AgCl;Cu(OH)2;BaSO4(Cu(OH)2和BaSO4可以互换)
(2)Ag++Cl-==AgCl↓;Cu2++2OH-==Cu(OH)2↓(或Ba2++SO42-==BaSO4↓)
本题解析:
本题难度:一般
3、填空题 (10分)有一透明溶液,可能含有 等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。
等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。
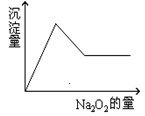
试推断:原溶液中一定含有?;一定没有?,可能含?,为了进一步确定可能含有的离子,应增加的实验操作为?,现象为?。
参考答案:Al3+、Mg2+? Fe3+、Cu2+、NH4+? K+
用洁净的铂丝蘸取待测液,在酒精灯上灼烧?火焰呈紫色
本题解析:加入Na2O2粉末只有无色无味的气体放出,说明没有NH4+。同时析出白色沉淀,则一定没有Fe3+和Cu2+。根据图像可知,生成的沉淀先增加,然后减少,最后不再发生变化,说明一定含有Al3+和Mg2+,最后生成的沉淀是氢氧化镁。钾离子无法确定,要进一步确定钾离子,可用通过焰色反应。
本题难度:一般
4、选择题 某无色溶液中,不能大量存在的离子是
A.MnO4-
B.K+
C.Al3+
D.NO3-
参考答案:A
本题解析:分析:溶液无色,则溶液中一定不存在有颜色的离子.
解答:A、MnO4-离子有颜色,故A选;
B、K+离子无色,故B不选;
C、Al3+离子无色,故C不选;
D、NO3-离子无色,故D不选.
故选A.
点评:本题考查离子共存问题,题目难度不大,注意常见离子的颜色.
本题难度:一般
5、选择题 下列反应既是离子反应,又是氧化还原反应的是
[? ]
A.氯化钠溶液中滴入硝酸银溶液
B.铁片置于氯化铜溶液中
C. 金属镁在氧气中燃烧
D.氢氧化铝与稀硫酸反应
参考答案:B
本题解析:
本题难度:简单