1、选择题 下列叙述正确的是( )
A.硅元素在自然界中以游离态存在
B.氨气是工业制取硝酸的重要原料
C.铝是金属,与强碱不能发生反应
D.陶瓷、玻璃、水泥都属于碳酸盐产品
参考答案:A、Si在自然界中的存在既有单质硅又有含硅的化合物,所以既有游离态又有化合态,故A错误;
B、氨气催化氧化可以获得一氧化氮,然后转化为二氧化氮,和水反应可以获得硝酸,氨气是工业制取硝酸的重要原料,故B正确;
C、金属铝既能和强酸反应又能和强碱反应,故C错误;
D、陶瓷、玻璃、水泥的主要成分中均含有硅酸盐,属于硅酸盐产品,故D错误.
故选B.
本题解析:
本题难度:简单
2、选择题 将一定量的镁铝合金样品分成两等份,一份加入足量NaOH溶液中,充分反应后,收集到标准状况下气体6.72L;另一份加入到足量稀盐酸中,充分反应后,收集到标准状况下气体11.2L。则原合金样品中镁的质量为
A.4.8 g
B.6 g
C.9.6 g
D.12 g
参考答案:C
本题解析:因为Al与HCl、NaOH反应生成的H2体积一样,所以Mg与HCl反应生成的气体为11.2-6.72L=4.48L,即0.2mol,Mg――H2,所以Mg为0.2mol即4.8g,所以原合金中Mg为9.6g
本题难度:一般
3、计算题 把一块镁铝合金投入到1mol/L盐酸中,待合金完全溶解后,再往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化如图所示。求:
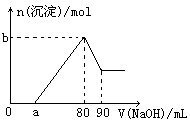
(1)盐酸的体积? (2)a的取值范围? (3)n(Mg2+)的取值范围
(4)当a值为30时,b值________________。
参考答案:(1) ?80mL (2分)?(2)? 0<a<50(3分)
(3)0 <n(Mg2+)<0.025mol ?(3分) (4) 0.02 (2分)
本题解析:略
本题难度:一般
4、简答题 (6分) 向1L AlCl3和FeCl3混合溶液中加入2mol /LNaOH溶液300mL时,产生的沉淀量达最大值;继续加入NaOH溶液,沉淀开始溶解,当加入NaOH溶液的总体积达到 350mL时,沉淀不再减少,求原溶液中FeCl3的物质的量浓度(需写出解题过程)。
参考答案:Al(OH)3 + NaOH = NaAlO2 + 2H2O
1mol?1mol
x? 2mol/L×(0.35L-0.3L)? x=0.1mol? (2分)
AlCl3 + 3NaOH = Al(OH)3 ↓+ 3NaCl
3mol? 1mol
y? 0.1mol? y=0.3mol? (2分)
FeCl3 + 3NaOH = Fe(OH)3 ↓+ 3NaCl
1mol? 3mol
z? (2mol/L×0.3L-0.3mol)? z=0.1mol
c(FeCl3)=0.1mol/1L=0.1mol/L? (2分)?答(略)
本题解析: 见答案
本题难度:一般
5、填空题 钠和铝是两种重要的金属。请回答:
(1)钠元素的金属性比铝的__________(填“强”或“弱”);常温下,可用________(填“钠”或“铝”)制成的容器盛装浓硫酸或浓硝酸。
(2)将一小块金属钠投入水中,发生反应的化学方程式为________________________;可观察到的实验现象是_____________(填序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)铝与氢氧化钠溶液反应的离子方程式为____________________________。
参考答案:(1)强;铝
(2)2Na+2H2O==2NaOH+H2↑;bc
(3)2Al+2OH-+2H2O==2AlO2-+3H2↑
本题解析:
本题难度:一般