1、计算题 (本题共15分)
有4种质量比可能相同或不同的镁铝合金样品①、②、③、④。甲、乙、丙、丁4位同学各取1种样品,进行下列实验,测定合金中镁的质量分数。
52.甲同学取样品①m1?g和过量的氢氧化钠溶液反应,然后过滤;再往滤液中通入过量的二氧化碳气体,将所得沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m1?g。则样品①合金中镁的质量分数为_____________。
53.乙同学取样品②m2?g和足量的盐酸反应,然后滴加过量的氢氧化钠溶液,将沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m2?g。则样品②合金中镁的质量分数为____________。
54.丙同学取样品③m3?g和足量的稀硫酸反应,发现固体完全溶解,标准状况下得到气体体积为V L,则样品③中m3的取值范围是___________________________________________。
丁同学取不同质量的样品④分别和30 mL同浓度的盐酸反应,所取合金质量与产生气体体积(已转化为标准状况)如下:
实验序号
| a
| b
| c
|
合金质量/mg
| 510
| 765
| 918
|
气体体积/mL
| 560
| 672
| 672
|
55.通过计算求该盐酸的物质的量浓度。
56.通过计算求样品④中合金中镁的质量分数。
57.在c组实验后,还需向容器中加入1.0 mol・L-1的氢氧化钠溶液多少毫升才能使剩余合金中的铝恰好完全溶解?
参考答案:
52.? 47.06% (2分)
53.? 60% (2分)
54.? 0.80V<m<1.07V
(2分,其它写法如27V/33.6<m<24V/22.4或9V/11.2<m<3V/2.8都给分)
55. 丙中盐酸反应完全,n(H2)="0.672/22.4" ="0.03" mol,(1分)
则c(HCl)="0.03×2/0.03=2.0" mol・L-1(1分)
56. 设合金中Mg、Al的物质的量分别为x、y,则有:
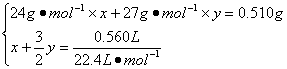
(1分)
解得:x =" y" =" 0.01" mol(1分)
则w(Mg)="[(0.01" mol×24 g・mol-1)/0.510 g]×100%=47.06%(1分)
57. 根据HCl ~ NaCl和Al ~ NaAlO2可知
n(NaCl)="n(HCl)=2.0" mol・L-1×0.030 L="0.06" mol(1分)
n(NaAlO2)="n(Al)=0.01" mol×918/510="0.018" mol(1分)
根据Na+守恒得:n(NaOH)="0.06" mol+0.018 mol="0.078" mol(1分)
故V(NaOH)="0.078" mol/1.0 mol・L-1="0.078" L="78" mL?(1分)
即c组实验后还需加入78 mL的氢氧化钠溶液,才能使剩余合金中的铝恰好完全溶解。
本题解析:52.镁铝合金中铝与氢氧化钠反应产物经过二氧化碳反应所得沉淀过滤、洗涤、烘干、灼烧,得到固体为氧化铝,反应前为镁铝反应后为铝和氧,质量不变,根据元素守恒可知氧化铝中氧的质量分数即为镁的质量分数,为16×3/(16×3+27×2)= 47.06%;53.该反应得到的固体为氧化镁,根据元素质量守恒,氧化镁中镁元素的质量分数即是镁铝合金中镁元素的质量分数,为24/(24+16)= 60%;
54.镁铝与稀硫酸反应消耗的硫酸不同产生的气体量也不同,故采用极值法确定其范围,金属全为镁时
金属的量为V /22.4×24=1.07V,金属全为铝时V? /22.4×2/3×27=0.80V,范围0.80V<m<1.07V;
55.丁同学实验数据中盐酸量固定,bc组盐酸反应完全,a组金属反应完全,故计算盐酸的浓度根据bc组气体数据直接得出,丙中盐酸反应完全,n(H2)="0.672/22.4" ="0.03" mol,
则c(HCl)="0.03×2/0.03=2.0" mol・L-1
56.根据a组数据列方程式可解,解法见答案;57.根据元素守恒,合金中铝最终变为NaAlO2,开始加入的盐酸最终变为氯化钠,此可称为终态分析法。
n(NaCl)="n(HCl)=2.0" mol・L-1×0.030 L="0.06" mol(氯原子守恒)
n(NaAlO2)="n(Al)=0.01" mol×918/510="0.018" mol(铝原子守恒)
根据Na+守恒得:n(NaOH)="0.06" mol+0.018 mol="0.078" mol
故V(NaOH)="0.078" mol/1.0 mol・L-1="0.078" L="78" mL?(1分)
即c组实验后还需加入78 mL的氢氧化钠溶液,才能使剩余合金中的铝恰好完全溶解。
本题难度:一般
2、实验题 为了检验市场上常见两种金属饮料瓶的主要成分,某小组取甲、乙两种饮料瓶,将其剪碎作为样品,分别按下述步骤进行实验:
I.取少量样品于试管中,加入盐酸,充分反应后过滤。
II.取少量滤液于试管中,向其中滴加氢氧化钠溶液。
步骤II的实验现象如下:
样品甲
| 生成白色沉淀,继续滴加氢氧化钠溶液,沉淀消失
|
样品乙
| 生成白色沉淀,白色沉淀迅速变为灰绿色,最终变为红褐色
|
?
(1)样品甲中金属的主要成分是?,生成白色沉淀反应的离子方程式是?。
(2)样品乙进行步骤I后所得滤液中一定含有的金属离子是?,白色沉淀变为红褐色反应的化学方程式是?。
参考答案:(1)Al? Al3++3OH―="=" Al(OH)3↓ (2)Fe2+? 4Fe(OH)2 + O2+2H2O == 4Fe(OH)3
本题解析:样品甲:2Al+6HCl=2AlCl3+3H2↑. AlCl3+3NaOH= Al(OH)3↓+3NaCl. Al(OH)3+OH-=AlO2-+ H2O;
样品乙: Fe+2HCl=FeCl2+H2↑. FeCl2+2NaOH= Fe(OH)2↓+3NaCl, 4Fe(OH)2 + O2+2H2O == 4Fe(OH)3
故样品甲中金属的主要成分是是铝,生成白色沉淀反应的离子方程式是Al3++3OH―="=" Al(OH)3↓(2)样品乙进行步骤I后所得滤液中一定含有的金属离子是Fe2+白色沉淀变为红褐色反应的化学方程式是: 4Fe(OH)2 + O2+2H2O == 4Fe(OH)3。
本题难度:一般
3、选择题 铝热反应(如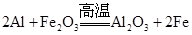 )中,铝的作用是( )
)中,铝的作用是( )
A.还原剂
B.氧化剂
C.催化剂
D.干燥剂
参考答案:A
本题解析:铝的化合价升高,失电子,是还原剂
本题难度:简单
4、填空题 铝的阳极氧化是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜,该氧化膜不溶于稀硫酸。
某化学研究小组在实验室中按下列步骤模拟铝表面“钝化”的产生过程。
(1)配制实验用的溶液。要配制200 mL密度为1.2 g/cm3的溶质质量分数为16%的NaOH溶液,需要称取________g NaOH固体。
(2)把铝片浸入热的16%的NaOH溶液中约半分钟左右洗去油污,除去表面的氧化膜,取出用水冲洗,写出除去氧化膜的离子方程式:________。
(3)按下图组装好仪器,接通开关K,通电约25 min。在阳极生成氧化铝,阴极产生气体。

写出该过程中的电极反应式:
阳极:_________________________________________;
阴极:_________________________________________。
(4)断开电路,取出铝片,用质量分数为1%的稀氨水中和表面的酸液,再用水冲洗干净。写出该过程发生反应的离子方程式:______________________。
参考答案:(1)38.4 (2)Al2O3+2OH-+3H2O=2[Al(OH)4]- (3)2Al+3H2O-6e-=Al2O3+6H+;6H++6e-=3H2↑ (4)NH3・H2O+H+=NH4++H2O
本题解析:(1)m[NaOH(aq)]=ρV=200 mL×1.2 g/cm3=240 g,m(NaOH)=m[NaOH(aq)]・w(NaOH)=240 g×16%=38.4 g。(2)铝片表面的氧化膜为Al2O3,是一种两性氧化物,可与强碱反应生成偏铝酸盐和水。(3)阳极是Al失去电子,与H2O共同作用转化成Al2O3;阴极是电解质溶液中的H+得到电子而转化成H2。(4)NH3・H2O属于弱碱,写离子方程式时要写成化学式的形式。
本题难度:一般
5、选择题 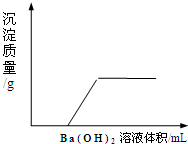 某溶液是由盐酸、稀硫酸、硫酸铁溶液、氯化铁溶液、稀硝酸、硝酸铁溶液几种中的两种混合而成,向该溶液中滴加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是
某溶液是由盐酸、稀硫酸、硫酸铁溶液、氯化铁溶液、稀硝酸、硝酸铁溶液几种中的两种混合而成,向该溶液中滴加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是
A.稀硝酸、氯化铁
B.稀硫酸、硝酸铁
C.稀硫酸、氯化铁
D.盐酸、硫酸铁
参考答案:A
本题解析:分析:依据向该溶液中滴加Ba(OH)2溶液的体积与生成沉淀的质量关系图象可知,开始无沉淀生成说明是中和酸的过程,因为硫酸钡难溶于酸,所以判断一定不含稀硫酸、硫酸铁溶液;其它物质可以是盐酸和氯化铁或硝酸铁形成的混合物,也可以是硝酸和氯化铁或硝酸铁形成的混合物.
解答:依据向该溶液中滴加Ba(OH)2溶液的体积与生成沉淀的质量关系图象可知,开始无沉淀生成说明是中和酸的过程,因为硫酸钡难溶于酸,判断一定不含稀硫酸、硫酸铁溶液;随着酸的反应完全会生成沉淀,证明一定含铁离子,形成沉淀为氢氧化铁;其它物质可以是盐酸和氯化铁或硝酸铁形成的混合物,也可以是硝酸和氯化铁或硝酸铁形成的混合物;
A、稀硝酸、氯化铁符合题意,故A正确;
B、加入氢氧化钡,开始无沉淀生成,一定不含硫酸,故B错误;
C、加入氢氧化钡,开始无沉淀生成,一定不含硫酸,故C错误;
D、加入氢氧化钡,开始无沉淀生成,一定不含硫酸铁,故D错误;
故选A.
点评:本题考查了物质性质的检验方法,明确图象中开始没有沉淀来确定溶液的成分是解答的关键,注意硫酸钡是不溶于酸的沉淀,题目难度不大.
本题难度:一般