1、实验题 为了测定某未知NaOH溶液的浓度,需要0.200mol・L-1的盐酸溶液500mL。某学生用实验室中常用的36.5%(密度为1.20g・cm-3)的浓盐酸配制所需稀盐酸,并设计了以下步骤完成实验。
⑴请你帮助该同学完成以下各步中的内容,并将其所设计的实验步骤正确排序。
A.用_____(从以下备选仪器中选取适当仪器,将其序号填入空格中)量取36.5%(密度为1.20g・cm-3)的浓盐酸________mL。
a.50mL量筒; b.10mL量筒; c.托盘天平。
B.将取好的浓盐酸在烧杯中加适量蒸馏水稀释。
C.轻轻振荡后继续加蒸馏水到液面距离仪器刻线1~2cm处。
D.等溶液恢复至室温。
E.将溶液用玻璃棒引流转入_________(填写所需仪器)中,再用适量蒸馏水洗涤烧杯和玻璃棒2~3次一并转入其中。
F.用胶头滴管加蒸馏水直到溶液液面恰好与刻线相切,塞好瓶塞摇匀即可。
以上各实验步骤的正确排列顺序是___________________________________。
⑵准确移取20.00mL待测NaOH溶液于锥形瓶中,用所配标准盐酸溶液进行滴定(以酚酞为指示剂)。滴定结果如下表:据此计算未知NaOH溶液的物质的量浓度为____________mol・L-1(精确到0.01)。

⑶下列操作或叙述正确的是_____(填写序号)。
A.滴定过程中,眼睛注视滴定管内溶液并使视线与液面的凹面水平。
B.滴定过程中由于摇动锥形瓶使少许溶液溅起沾在瓶内壁,为使测定结果正确,可用少许蒸馏水将其冲入锥形瓶内的溶液中。
C.容量瓶和滴定管在使用前洗净后都要检查是否漏液。
D.向锥形瓶中移取NaOH溶液前,用少许NaOH溶液润洗锥形瓶2~3次。
⑷下列操作或现象会导致测定结果偏高的是_________(填写序号)。
A.滴定过程中不小心将一滴溶液滴在锥形瓶外;
B.滴定结束时,发现在滴定管尖嘴处有小气泡;
C.滴定结束后仰视滴定管液面读数;
D.溶液褪色立即读数,摇动锥形瓶后看到溶液红色复出;
E.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗,直接加入标准液进行滴定。
参考答案:⑴ b;8.4mL;500mL容量瓶;ABDECF
⑵0.22
⑶BC
⑷ACE
本题解析:
本题难度:一般
2、选择题 用NA表示阿伏加德罗常数的值。下列说法正确的是(?)
A.标准状况下,22.4 L乙醇中含有的碳原子数目为2NA
B.1 mol CnH2n含有的共用电子对数为(3n+1)NA
C.1 mol CO2与1 mol Na2O2完全反应时,转移的电子数目为NA
D.1 mol・L-1的FeCl3溶液中,所含Fe3+的数目小于NA
参考答案:C
本题解析:A项,标况下,乙醇为液体,错误;B项,1 mol CnH2n中应含有共用电子对数为3nNA,错误;D项,未指明溶液的体积;C项,Na2O2既是氧化剂又是还原剂,正确。
本题难度:一般
3、选择题 下列溶液中,c (Cl-)最小的是
[? ]
A.20 mL 0.5 mol/L AlCl3溶液
B.30 mL 1 mol/L KCl溶液
C.7.5 mL 2 mol/L MgCl2溶液
D.10 mL 3 mol/L NaCl溶液
参考答案:B
本题解析:
本题难度:简单
4、计算题 Na2O2曾经是潜水艇或航天器中最理想的供氧剂。下表是人体呼出气体的成分(均为体积百分含最)。
?
| 空气
成分
| 人体呼出
气体成分
|
N2
| 78%
| ? 74%
|
O2
| 21%
| ? 16%
|
H2O
| 0. 5%
| ? 6%
|
CO2
| 0. 03%
| ? 4%
|
?
(1)已知一个人一天大约要产生16 mol CO2。若全部被Na2O2吸收,需要Na2O2________ g。
(2)若要使被吸收的CO2与产生的O2体积相等,就需
要在Na2O2中添加KO2.计算要达到该目的.Na2O2与KO2的物质的量比例是?。
已知:4KO2+2CO2=2K2CO3+3O2
(3)计算100 L空气经过人体呼吸后,呼出气体中O2的体积(标准状况下,保留2位小数)____?L。
(4)为保持航天器中空气成分恒定,并充分利用资源,需对人体呼出的气体进行处 理,无用物质排出航天器。100 L空气经过人体呼吸后,欲使呼出的气体经过处理后恢复原空气成分且体积仍为100 L(可供使用的化学试剂只有Na2O2).通过计算回答:若先利用CO2,还需要利用水蒸气,求需要水蒸气体积?L。
参考答案:(1)1248?
(2)n(Na2O2):n(KO2)=1:2?(3)V(O2)=16.86L
(4)4.10
本题解析:
(1)过氧化钠和二氧化碳的反应方程式为:2Na2O2+2CO2=2Na2CO3+O2,设需要过氧化钠的质量为x,
2Na2O2+2CO2=2Na2CO3+O2
156g? 2mol
x? 16mol
x=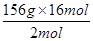 =1248g
=1248g
(2)Na2O2和 CO2反应方程式为:2Na2O2+2CO2=2Na2CO3+O2, KO2和 CO2反应方程式为:4KO2+2CO2=2K2CO3+3O2,根据反应方程式知,要使被吸收的CO2与产生的O2体积相等,则参加反应的n(Na2O2):n(KO2)=2:4=1:2
(3)呼吸前后,氮气不参加反应,所以氮气的量不变,呼入的气体中氮气体积=100L×78%=78L,氮气的量不变,所以呼出的气体体积=78L÷74%=105.4L,所以V(O2)=78L/74%×16%=16.86L。
(4)呼入气体中氧气的体积=100L×21%=21L,呼出的气体中氧气的体积是16.86L,所以氧气体积减少为(21-16.86)L=4.14L?O2。
二氧化碳气体增加的量=78L/74%×4%-100L×0.03%=4.22L-0.03L=4.19L,将增加的CO2用Na2O2吸收,生成O2是二氧化碳的一半为2.095L,为补足减少的4.14L?O2,还需要2.045L?O2,则需要用Na2O2吸收 H2O体积为氧气的2倍=2.045L×2=4.09L,剩余的水=6.32L-4.09L=1.73L液化回收。还需要水蒸气参加反应,需要水蒸气的体积是4.10L
本题难度:一般
5、填空题 等物质的量的CO和CO2中所含O原子个数之比?,C原子数之比?,二者的质量之比?,在同温同压下的体积之比?。
参考答案:1:2,? 1:1,? 7:11, 1:1
本题解析:CO和CO2防止分别含有1个氧原子和2个氧原子,所以等物质的量的CO和CO2中所含O原子个数之比1:2;同样分析可知,等物质的量的CO和CO2中所含C原子数之比1:1;根据m=nM可知,二者的质量之比是28:44=7:11;根据阿伏加德罗定律可知,相同体积的任何气体含有相同数目的分子,则在同温同压下的体积之比1:1。
点评:该题是高考中的常见题型,属于基础性试题的考查,难度不大。明确组成气体分子的原子数目,以及灵活运用阿伏加德罗定律是答题的关键。
本题难度:一般