1、计算题 (6分)某2 .0 L硫酸溶液中含有1.0 mol H2SO4。试计算:
(1)溶液中H2SO4的物质的量浓度;
(2)向上述溶液中加入足量的铁粉,产生气体的体积(标准状况);
(3)假设反应前后溶液体积不变,则所得溶液中Fe2+的物质的量浓度。
2、计算题 (8分)标准状况下11.2 L HCl溶于水形成500 mL 溶液。
(1)所得盐酸的物质的量浓度为?;
(2)向其中加入??g NaOH才能中和完全;
(3)若不考虑加入NaOH对体积造成的影响,所得NaCl的物质的量浓度为?;
(4)再向其中加入??mL 密度为1.7 g/cm3,质量分数为25%的AgNO3溶液可使Cl-完全沉淀。
3、选择题 下列各物质所含原子个数,按照由多到少顺序排列的是( )
①标况下22.4L氦气?②4℃时,9ml水?③0.2mol磷酸?④0.5mol氨气.
A.①④③②
B.④③②①
C.②③④①
D.①④②③
4、简答题 把5.85g?NaCl配成100mL溶液,求其物质的量浓度.该溶液能与多少升0.100mol?L-1AgNO3溶液完全反应?
5、计算题 19.2g Cu与过量的50 mL 18 mol・L-1浓硫酸加热完全反应后,
反应方程式如下: Cu + 2H2SO4(浓)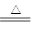 CuSO4?+ SO2↑+ 2H2O 。
CuSO4?+ SO2↑+ 2H2O 。
(1)得到SO2气体的体积(标准状况下)是?L;
(2)若反应后溶液中加入水至溶液的体积为500mL,取出50mL,那么50mL溶液中CuSO4?的物质的量浓度为?mol・L-1;
(3)往反应后溶液中加入足量的BaCl2,可以生成硫酸钡沉淀为?g。