|
高考化学知识点整理《水的电离平衡》试题巩固(2020年最新版)(十)
2021-06-11 05:52:31
【 大 中 小】
|
1、填空题 工业废水随意排放会造成严重污染,根据成分不同可采用不同的处理方法。
(1)电池生产工业废水中常含有Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去。已知室温下Ksp(FeS)=6.3×10-18mol2・L-2,Ksp(CuS)=1.3×10-36mol2・L-2。
①请用离子方程式说明上述除杂的原理 。
②FeS高温煅烧产生的SO2气体通入下列溶液中,能够产生沉淀的是 (填序号)
A.Ba(NO3)2
B.BaCl2
C.Ba(OH)2
D.溶有NH3的BaCl2溶液
| ③若将足量SO2气体通入0.2 mol・L-1的NaOH溶液,所得溶液呈酸性,则溶液中离子浓度由大到小的顺序为 。
(2)采用电解法处理含有Cr2O72-的酸性废水,在废水中加入适量NaCl,用铁电极电解一段时间后,有Cr(OH)3和Fe(OH)3沉淀生成,从而降低废水中铬元素的含量。若阳极用石墨电极则不能产生Cr(OH)3沉淀,用必要的化学语言说明原因___________________。
(3)废氨水可以转化成氨,氨再设计成碱性燃料电池。如图是该燃料电池示意图,产生的X气体可直接排放到大气中。a电极作 极(填“正”“负”“阴”或“阳”),其电极反应式为 ;T℃下,某研究员测定NH3・H2O的电离常数为1.8×10-5,NH4+的水解平衡常数为1.5×10-8(水解平衡也是一种化学平衡,其平衡常数即水解常数),则该温度下水的离子积常数为 ,请判断T 25℃(填“>”“<”“=”)。

参考答案:(1)①FeS(s)+Cu2+(aq)=" CuS(s)+" Fe 2+(aq)
②A C D
③c(Na+)>c(HSO3-)> c (H+)>c(SO32-)> c(OH-)。
(2)因为Fe电极在电解过程中产生还原性的Fe2+,将溶液中Cr2O72-还原为Cr3+,Cr2O72-+6Fe2++14H+ =2Cr3++6Fe3++7H2O。若改用石墨电极,阳极产生的是Cl2,不能将Cr2O72-还原为Cr3+。
(3)负 2NH3+6OH--6e- =N2+6H2O 2.7×10-13;>
本题解析:(1) FeS尽管难溶,也有一定的溶解度,在溶液中存在着沉淀溶解平衡:FeS(s) Fe2+(aq)+S2-(aq) ,由于Ksp(FeS)=6.3×10-18mol2・L-2>>Ksp(CuS)=1.3×10-36mol2・L-2,所以当溶液中含有Cu2+时,Cu2+就会与FeS电离产生的S2-结合产生更难溶的沉淀CuS。Cu2++ S2-=CuS↓,FeS再溶解电离,产生的S2-再反应变为CuS沉淀。最终能够把溶液中的Cu2+完全沉淀除去。反应的两种方程式为:①FeS(s)+Cu2+(aq)=" CuS(s)+" Fe 2+( aq). ② SO2+H2O=H2SO3,溶液显酸性。A.当向其中加入Ba(NO3)2时,也就相当于存在硝酸。硝酸有强氧化性,能把H2SO3氧化产生H2SO4.故会产生BaSO4沉淀。正确。B.假如能与BaCl2发生反应,则反应的方程式为:B.BaCl2+ SO2+H2O=BaSO3↓+2HCl. BaSO3能与HCl发生反应,所以在酸性环境不存在。即该反应是不能发生的。换句话说就是不能发生反应产生沉淀。C.酸性氧化物SO2能与碱发生反应:Ba(OH)2+ SO2=BaSO3↓+ H2O.正确。D.首先发生反应:2NH3+ SO2+H2O= (NH4)2SO3,然后发生:(NH4)2SO3+BaCl2= BaSO3↓+ 2NH4Cl .正确。因此选项为A、C、D。③由于SO2足量。所以反应的方程式为:SO2+NaOH=NaHSO3。NaHSO3=Na++HSO3-。HSO3-在溶液中存在电离平衡HSO3- Fe2+(aq)+S2-(aq) ,由于Ksp(FeS)=6.3×10-18mol2・L-2>>Ksp(CuS)=1.3×10-36mol2・L-2,所以当溶液中含有Cu2+时,Cu2+就会与FeS电离产生的S2-结合产生更难溶的沉淀CuS。Cu2++ S2-=CuS↓,FeS再溶解电离,产生的S2-再反应变为CuS沉淀。最终能够把溶液中的Cu2+完全沉淀除去。反应的两种方程式为:①FeS(s)+Cu2+(aq)=" CuS(s)+" Fe 2+( aq). ② SO2+H2O=H2SO3,溶液显酸性。A.当向其中加入Ba(NO3)2时,也就相当于存在硝酸。硝酸有强氧化性,能把H2SO3氧化产生H2SO4.故会产生BaSO4沉淀。正确。B.假如能与BaCl2发生反应,则反应的方程式为:B.BaCl2+ SO2+H2O=BaSO3↓+2HCl. BaSO3能与HCl发生反应,所以在酸性环境不存在。即该反应是不能发生的。换句话说就是不能发生反应产生沉淀。C.酸性氧化物SO2能与碱发生反应:Ba(OH)2+ SO2=BaSO3↓+ H2O.正确。D.首先发生反应:2NH3+ SO2+H2O= (NH4)2SO3,然后发生:(NH4)2SO3+BaCl2= BaSO3↓+ 2NH4Cl .正确。因此选项为A、C、D。③由于SO2足量。所以反应的方程式为:SO2+NaOH=NaHSO3。NaHSO3=Na++HSO3-。HSO3-在溶液中存在电离平衡HSO3- H++SO32-和水解平衡HSO3-+ H2O H++SO32-和水解平衡HSO3-+ H2O  H2SO3+OH-。电离使溶液显酸性,水解使溶液显碱性。因为所得溶液呈酸性,所以电离大于水解。c (H+)>c(OH-).在溶液中除了存在水解平衡外还存在H2O H2SO3+OH-。电离使溶液显酸性,水解使溶液显碱性。因为所得溶液呈酸性,所以电离大于水解。c (H+)>c(OH-).在溶液中除了存在水解平衡外还存在H2O  H++OH-,SO32-只有HSO3-电离产生,所以c (H+)>c(SO32-)。电解质的电离程度:HSO3-> H2O。因此c(SO32-)> c(OH-)。无论HSO3-是电离还是水解都要消耗,所以c(Na+)>c(HSO3-).因此溶液中各种离子的浓度关系为:c(Na+)>c(HSO3-)> c (H+)>c(SO32-)> c(OH-)。(2) 用铁电极电解一段时间后, Fe(OH)3沉淀生成,说明Fe与电源的正极相连接,作阳极,被氧化发生还原反应:Fe-2e-=Fe2+.产生的Fe2+有还原性,能将溶液中Cr2O72-还原为Cr3+,二者发生的反应为:Cr2O72-+6Fe2++14H+ =2Cr3++6Fe3++7H2O,Cr3+与Fe3+水解产生Cr(OH)3和Fe(OH)3沉淀,从而可以降低废水中铬元素的含量。若阳极用石墨电极,则电极本身不参加反应,是溶液中的Cl-失去电子。在阳极产生的是Cl2,就不能将Cr2O72-还原为Cr3+。(3)氨设计成碱性燃料电池,产生的X气体可直接排放到大气中。则X为N2,a电极作负极,电极反应为2NH3+6OH--6e- =N2+6H2O。通入空气的电极为正极,发生反应:O2+4e-+2H2O=4OH-。NH3・H2O H++OH-,SO32-只有HSO3-电离产生,所以c (H+)>c(SO32-)。电解质的电离程度:HSO3-> H2O。因此c(SO32-)> c(OH-)。无论HSO3-是电离还是水解都要消耗,所以c(Na+)>c(HSO3-).因此溶液中各种离子的浓度关系为:c(Na+)>c(HSO3-)> c (H+)>c(SO32-)> c(OH-)。(2) 用铁电极电解一段时间后, Fe(OH)3沉淀生成,说明Fe与电源的正极相连接,作阳极,被氧化发生还原反应:Fe-2e-=Fe2+.产生的Fe2+有还原性,能将溶液中Cr2O72-还原为Cr3+,二者发生的反应为:Cr2O72-+6Fe2++14H+ =2Cr3++6Fe3++7H2O,Cr3+与Fe3+水解产生Cr(OH)3和Fe(OH)3沉淀,从而可以降低废水中铬元素的含量。若阳极用石墨电极,则电极本身不参加反应,是溶液中的Cl-失去电子。在阳极产生的是Cl2,就不能将Cr2O72-还原为Cr3+。(3)氨设计成碱性燃料电池,产生的X气体可直接排放到大气中。则X为N2,a电极作负极,电极反应为2NH3+6OH--6e- =N2+6H2O。通入空气的电极为正极,发生反应:O2+4e-+2H2O=4OH-。NH3・H2O  NH4++OH-, NH4++OH-, 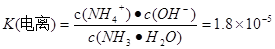 - NH4++ H2O - NH4++ H2O 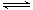 H+ + NH3・H2O, H+ + NH3・H2O,  .将两式相乘,可得 .将两式相乘,可得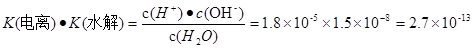 。c (H+)・c(OH-)=K(电离) ・K(水解) ・c(H2O)="Kw." 所以在该温度下水的离子积常数Kw=2.7×10-13.水是弱电解质,升高温度,促进水的电离,水电离产生的离子浓度增大,水的离子积常数也增大。由于2.7×10-13>1.0×10-14.所以温度高于25℃。 。c (H+)・c(OH-)=K(电离) ・K(水解) ・c(H2O)="Kw." 所以在该温度下水的离子积常数Kw=2.7×10-13.水是弱电解质,升高温度,促进水的电离,水电离产生的离子浓度增大,水的离子积常数也增大。由于2.7×10-13>1.0×10-14.所以温度高于25℃。
考点:考查沉淀的转化、SO2的除去方法、含有Cr2O72-的酸性废水的电解法处理、原电池的反应原理及电极式的书写、弱电解质的电离平衡、盐的水解平衡、水的离子积常数的计算的知识。
本题难度:困难
2、填空题 (16分)钢厂酸洗废液(成分如下表所示)在工业生产中还具有很多用途。
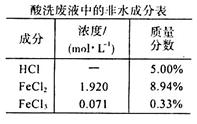
(1)欲检验该酸洗废液中含有的少量Fe3+,最宜选用的试剂是_____溶液;为检验其中的Fe2+,某同学设计了如下实验:取该酸洗废液少许加入试管中,滴入几滴酸性KMnO4溶液后发现紫色消失。该同学得出结论:该溶液中含有Fe2+。大家认为该同学的实验设计不合理,理由是____________________________(用必要的文字和离子方程式解释)。
(2)采用石墨作电极电解上述酸洗废液时,初始阶段,阳极板上有气泡生成,此时与该现象有关的阳极电极反应式为______;向上述酸洗废液中加入KOH溶液中和后,在合适的电压下电解,可在__________(填“阴”或“阳”)极生成高铁酸钾(K2FeO4)。
(3)利用上述酸洗废液、含铝矿石(主要成分为Al2O3、Fe2O3和SiO2)以及新制的硅酸(活化硅酸),制备聚硅酸氯化铝铁絮凝剂(简称PAFSC),具体方法如下:
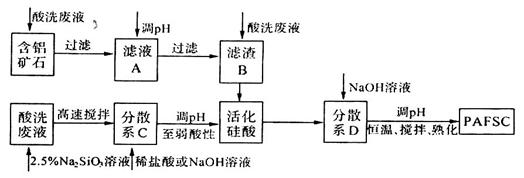
①适当调高滤液A的pH,Al3+和Fe2+转化为沉淀,原因是______________(请用沉淀溶解平衡的理论解释)。
②PAFSC絮凝剂净化水的过程中,Al3+参与反应的离子方程式为________________。
③25℃时,PAFSC的除浊效果随溶液pH的变化如图所示(图中的NTU为浊度单位),则在下列pH范围中,PAFSC除浊效果最佳的是______(填下列序号字母)。
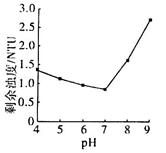
a.4~5 b.5~7 c.7~8 d.8~9
25℃时,pH>7且随pH增大,PAFSC的除浊效果明显变差,原因是碱性增强,使胶体发生了_____现象。
参考答案:(1)(5分)KSCN;酸性KMnO4溶液会氧化Cl-,导致紫色消失,
2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O(3分)
(2)(4分)2Cl--2e-=Cl2↑;阳
(3)(7分)①调高溶液pH,溶液中[OH-]增大,从而使Al(OH)3和Fe(OH)3的Qc大于其Ksp
(或调高溶液pH,溶液中[OH-]增大,从而使Al(OH)3和Fe(OH)3的沉淀溶解平衡向沉淀方向移动)
②Al3++3H2O=Al(OH)3(胶体)+3H+
③b;聚沉(1分)
本题解析:(1)检验该酸洗废液中含有的少量Fe3+,最宜选用的试剂是KSCN溶液;该酸性废液中的Fe2+、Cl-均有还原性,都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,该同学的实验设计不合理,理由是酸性KMnO4溶液会氧化Cl-,导致紫色消失,2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O。(2)用石墨作电极电解酸洗废液时,初始阶段,阳极板上Cl-放电生成氯气,电极反应式为2Cl--2e-=Cl2↑;向上述酸洗废液中加入KOH溶液中和后,在合适的电压下电解,Fe3+、Fe2+转化为FeO42―,化合价升高发生氧化反应,可在阳极生成高铁酸钾(K2FeO4)。(3)① 适当调高滤液A的pH,Al3+和Fe2+转化为沉淀,原因是调高溶液pH,溶液中[OH-]增大,从而使Al(OH)3和Fe(OH)3的Qc大于其Ksp。②PAFSC絮凝剂净化水的过程中,Al3+参与反应的离子方程式为Al3++3H2O=Al(OH)3(胶体)+3H+。③分析题给图像知,25℃时pH在5~7时PAFSC的除浊效果最佳,选b。25℃时,pH>7且随pH增大,PAFSC的除浊效果明显变差,原因是碱性增强,使胶体发生了聚沉现象。
考点:以钢厂酸洗废液的再利用为载体考查离子检验,化学实验方案的分析、评价,电解原理,胶体的性质和应用及图像分析能力。
本题难度:困难
3、选择题 下列电离方程式书写正确的是( ? )
A.NH3?H2O=NH4++OH-
B.H2SO4=2H++SO42-
C.NaHCO3=Na++H++CO32-
D.KClO3=K++Cl-+302-
参考答案:B
本题解析:
本题难度:一般
4、选择题 水的电离过程为H2O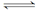 H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14, K(35℃)=2.1×10-14。则下列叙述正确的是( ) H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14, K(35℃)=2.1×10-14。则下列叙述正确的是( )
A.c(H+)随着温度升高而降低
B.35℃时,c(H+)>c(OH-)
C.水的电离度 > >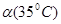
D.水的电离是吸热的
| 
 <
<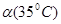 ,故C错误;升高温度,水的离子积常数增大,说明水的电离程度增大,则水的电离过程是吸热的,故D正确;故选D.
,故C错误;升高温度,水的离子积常数增大,说明水的电离程度增大,则水的电离过程是吸热的,故D正确;故选D.