|
|
|
高考化学知识点整理《水的电离平衡》试题巩固(2020年最新版)(九)
2021-06-11 05:52:31
【 大 中 小】
|
1、填空题 工业废水随意排放会造成严重污染,根据成分不同可采用不同的处理方法。
(1)电池生产工业废水中常含有Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去。已知室温下Ksp(FeS)=6.3×10-18mol2・L-2,Ksp(CuS)=1.3×10-36mol2・L-2。
①请用离子方程式说明上述除杂的原理 。
②FeS高温煅烧产生的SO2气体通入下列溶液中,能够产生沉淀的是 (填序号)
A.Ba(NO3)2
B.BaCl2
C.Ba(OH)2
D.溶有NH3的BaCl2溶液
| ③若将足量SO2气体通入0.2 mol・L-1的NaOH溶液,所得溶液呈酸性,则溶液中离子浓度由大到小的顺序为 。
(2)采用电解法处理含有Cr2O72-的酸性废水,在废水中加入适量NaCl,用铁电极电解一段时间后,有Cr(OH)3和Fe(OH)3沉淀生成,从而降低废水中铬元素的含量。若阳极用石墨电极则不能产生Cr(OH)3沉淀,用必要的化学语言说明原因___________________。
(3)废氨水可以转化成氨,氨再设计成碱性燃料电池。如图是该燃料电池示意图,产生的X气体可直接排放到大气中。a电极作 极(填“正”“负”“阴”或“阳”),其电极反应式为 ;T℃下,某研究员测定NH3・H2O的电离常数为1.8×10-5,NH4+的水解平衡常数为1.5×10-8(水解平衡也是一种化学平衡,其平衡常数即水解常数),则该温度下水的离子积常数为 ,请判断T 25℃(填“>”“<”“=”)。

2、填空题 (16分)钢厂酸洗废液(成分如下表所示)在工业生产中还具有很多用途。
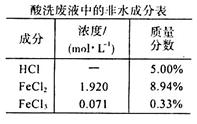
(1)欲检验该酸洗废液中含有的少量Fe3+,最宜选用的试剂是_____溶液;为检验其中的Fe2+,某同学设计了如下实验:取该酸洗废液少许加入试管中,滴入几滴酸性KMnO4溶液后发现紫色消失。该同学得出结论:该溶液中含有Fe2+。大家认为该同学的实验设计不合理,理由是____________________________(用必要的文字和离子方程式解释)。
(2)采用石墨作电极电解上述酸洗废液时,初始阶段,阳极板上有气泡生成,此时与该现象有关的阳极电极反应式为______;向上述酸洗废液中加入KOH溶液中和后,在合适的电压下电解,可在__________(填“阴”或“阳”)极生成高铁酸钾(K2FeO4)。
(3)利用上述酸洗废液、含铝矿石(主要成分为Al2O3、Fe2O3和SiO2)以及新制的硅酸(活化硅酸),制备聚硅酸氯化铝铁絮凝剂(简称PAFSC),具体方法如下:
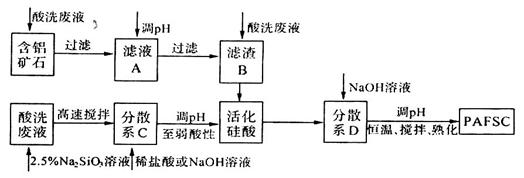
①适当调高滤液A的pH,Al3+和Fe2+转化为沉淀,原因是______________(请用沉淀溶解平衡的理论解释)。
②PAFSC絮凝剂净化水的过程中,Al3+参与反应的离子方程式为________________。
③25℃时,PAFSC的除浊效果随溶液pH的变化如图所示(图中的NTU为浊度单位),则在下列pH范围中,PAFSC除浊效果最佳的是______(填下列序号字母)。
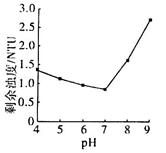
a.4~5 b.5~7 c.7~8 d.8~9
25℃时,pH>7且随pH增大,PAFSC的除浊效果明显变差,原因是碱性增强,使胶体发生了_____现象。
3、选择题 下列电离方程式书写正确的是( ? )
A.NH3?H2O=NH4++OH-
B.H2SO4=2H++SO42-
C.NaHCO3=Na++H++CO32-
D.KClO3=K++Cl-+302-
4、选择题 水的电离过程为H2O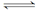 H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14, K(35℃)=2.1×10-14。则下列叙述正确的是( ) H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14, K(35℃)=2.1×10-14。则下列叙述正确的是( )
A.c(H+)随着温度升高而降低
B.35℃时,c(H+)>c(OH-)
C.水的电离度 > >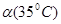
D.水的电离是吸热的
|
5、选择题 常温下,pH=3的醋酸溶液和pH=11的NaOH溶液混合,下列有关说法中一定正确的是
[? ]
A.水电离出的氢离子浓度:NaOH溶液>醋酸溶液
B.pH=3的醋酸溶液中存在:c(CH3COOH)+ c(CH3COO-)= 10-3 mol/L
C.反应后的溶液中存在:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.反应后的溶液中存在:c(CH3COO-)+c(OH-)=c(Na+)+c(H+)
