|
|
|
高考化学知识点整理《水的电离平衡》试题巩固(2020年最新版)(六)
2021-06-11 05:52:31
【 大 中 小】
|
1、选择题 下列方程式书写正确的是
[? ]
A.HCO3-在水溶液中的电离方程式:HCO3-+H2O H3O++CO32- H3O++CO32-
B.H2SO3的电离方程式H2SO3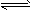 2H++SO32- 2H++SO32-
C.CO32-的水解方程式:CO32-+2H2O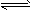 H2CO3+2OH- H2CO3+2OH-
D.CaCO3的电离方程式:CaCO3=Ca2++CO32-
参考答案:AD
本题解析:
本题难度:简单
2、选择题 下列说法或表示方法正确的是
[? ]
A.在稀溶液中,H+(aq)+ OH-(aq)= H2O(l) △H=-57.3 kJ・mol-1,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热大于57.3kJ
B.由C(石墨)= C(金刚石) △H=+1.90 kJ/mol可知金刚石比石墨稳定
C.相同温度下,①pH=5的NH4Cl溶液、②pH=4的稀盐酸中由水电离出的c(H+):①<②
D.pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+) > c(CH3COO-)
参考答案:A
本题解析:
本题难度:一般
3、选择题 常温时,在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH- 离子浓度分别为Amol/L与Bmol/L,则A和B关系为 ( )
A.A>B
B.A=10-4 B
C.B=10-4 A
D.A=B
|
参考答案:B
本题解析:酸和碱都抑制水的电离,能水解的盐促进水的电离,NaOH自身能电离出OH-,所以溶液中的H+是水电离出来的,因此水电离的OH-为10-9mol/L,CH3COONa自身不能电离出OH-,所以溶液中的OH-都是水电离出来的,因此水电离的OH-为10-5mol/L。所以A=10-4 B,答案选B。
考点:考查水电离的离子浓度的计算。
本题难度:一般
4、选择题 下列关于电解质溶液的正确判断是
[? ]
A.在pH=12的溶液中,K+、Cl-、HCO3-、Na+可以大量共存
B.在pH=0的溶液中,Na+、NO3-、SO32-、K+可以大量共存
C.由0. 1mol/L 一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH= B++OH-
D.由0. 1mol/L一元酸HA溶液的pH=3,可推知NaA溶液存在A-+H2O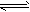 HA+OH- HA+OH-
参考答案:D
本题解析:
本题难度:一般
5、实验题 (10分)某种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定如下:
①需配制0.1 mol?L-1的盐酸和0.1mol?L-1的氢氧化钠溶液;
②每次取一粒(药片质量均相同)0.2g的此胃药片,磨碎后加入20.00mL蒸馏水;
③以酚酞为指示剂,用0.1mol?L-1的氢氧化钠溶液滴定,需用去VmL达滴定终点;
④加入25.00mL0.1mol?L-1的盐酸溶液。
(1)写出实验过程中第一次滴定①-④的编号顺序______________。
(2)下图所示的仪器中配制0.1mol?L-1盐酸和0.1mol?L-1氢氧化钠溶液肯定不需要的仪器是(填序号)_________,配制上述溶液还需要的玻璃仪器是(填仪器名称)__________。
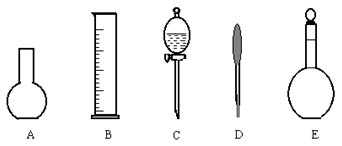
(3)配制上述溶液应选用的容量瓶的规格是(重复滴定一次)__________________。
A.50mL、50mL
B.100mL、100mL
C.100mL、150mL
D.250mL、250mL
|
(4)写出有关的化学方程式_____________________
。
参考答案:(1)①②④③(或②①④③)。(2)A、C;玻璃棒、烧杯。(3)B。
(4)CaCO3+2HCl=CaCl2+CO2+H2O HCl+NaOH=NaCl+H2O
本题解析:(1)首先配制需要的标准浓度的溶液,取待测物制成溶液,在待测物溶液中加入一定量的盐酸,再用氢氧化钠进行滴定,所以顺序为:①②④③(或②①④③)。(2)配制溶液需要容量瓶,量筒,胶头滴管,烧杯,玻璃棒,不需要平底烧瓶和分液漏斗,所以选A、C;图上还缺少玻璃棒、烧杯。(3)因为每次实验至少使用25毫升溶液,两次就需要50毫升,所以至少需要配制溶液各100毫升,选B。(4)过程中涉及了碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,盐酸和氢氧化钠反应生成氯化钠和水,所以方程式为:(4)CaCO3+2HCl=CaCl2+CO2+H2O HCl+NaOH=NaCl+H2O
考点:酸碱中和滴定。
本题难度:一般